線維筋痛症(FM)
線維筋痛症(fibromyalgia: FM)とは
とにかく、いつも全身が痛い、こわばるように痛い。いつまでも続く、刺されたような痛み、切られたような痛み、じりじりした痛み、ズーンとした重い痛み、突然襲いかかる激しい痛み。
全身が重い。重しが全身にいつも乗っているよう。水の中で生活しているよう。少しでも活動すると、何日も回復しない。
物忘れがひどい。思考力がおちている。頭がぼーっとする。
お腹の調子も悪い。
他にもいろいろな身体の症状がありすぎて説明できない。
気分が、わけもなく落ち込む。わけもなく不安になる。眠れない。寝付きが悪い。寝付いてもすぐに起きてしまう。
あまりのつらさで、のたうち回っていても‥‥‥誰も理解しようとしてくれない。誰にも理解されない。ときには、心ない言葉を投げかけられ、時に精神論でかたづれられてしまう。軽くあしらわれてしまう。
これだけ、辛いのに、社会は理解してくれない。社会的保障もない。社会支援も期待できない。かえって心ない対応をされてしまう。軽くあしらわれてしまう。
★比較的重症の方は上記のような症状、心理状態、社会的状況で苦しんでいます。

本邦の線維筋痛症ガイドライン2017によると
「線維筋痛症(FM)は、からだの広い部位に、筋肉や関節の慢性の痛みとこわばりを主な症状とし、
明らかな部位に圧痛(おすと起きる強い痛み)以外に、一般的な検査所見に異常がなく、
治療抵抗性(治療しても改善することがむずかしい)であり、
疲労感、睡眠障害や抑うつ気分(落ち込んだ気持ち)などの多彩な身体および精神・神経症状を伴い、
中年以降の女性に多く起きる原因不明のリウマチ性疾患である。」
とあります。

線維筋痛症(FM)は全身の痛みがつらく長く続いてしまう疾患ですが、自分以外の人や、医師にまでも理解されないことが多く、孤独な闘いを強いられます。
FMは、いまだに、その病因、病態の解明、治療法の確立が遅れており、この疾患の診療医療機関は全国的に数が少ないようです。
整形外科外来では、肩こり、腰痛などの痛みの患者さんの中に、線維筋痛症(FM)の患者さんがしばしば存在します。わが国の報告において、2011年の改定診断基準(Wolfら)を満たした患者のうち、医療施設を受診しFMと診断されたのはわずか2.5%であったと報告しました(Nakamura Iら)。
またFMは過小診断や誤診されることの多い疾患であり主に診断基準および治療法などの医学的な不確実性が影響していると報告されています(Hauser Wら)。
さらに医師側の原因として、
1、FMの認識と診断について十分な知識を持っていない可能性がある。
2、FMに対するスティグマを考慮し、診断を下すことを避けている可能性がある。
3、臨床診断を確認するための検査での客観的異常やバイオマーカーによる判断に慣れており、
FMなどのFSSに対する心理社会的アプローチや症状に基づく診断の不確実性に対する消極性の可能性がある。
4、FMは「存在しない」という考えによる可能性などを挙げています。
・日本線維筋痛症学会,日本医療研究開発機構線維筋痛症研究班:線維筋痛症診療ガイドライン2017.日本医事新報社,東京,pp4-9, 2017
・Nakamura: I,: Nishioka K, Usui C et al: An epidemiologic internet survey of fibromyalgia and chronic pain in Japan. Arthritis Care Res (Hoboken) 66: 1093-1101, 2014
・Häuser: W,: Puttini PS, Fitzcharles MA: Fibromyalgia syndrome: under-, over- and misdiagnosis. Clin Exp Rheumatol 37: 90-97, 2019

線維筋痛症(FM)世界啓発デー
近代看護の道を切り開いた、フローレンス・ナイチンゲールの生誕日である、5月12日に、線維筋痛症(FM)、筋痛性脳脊髄炎/慢性疲労症候群(ME/CFS)、化学物質過敏症(multiple chemical sensitivity:MCS)が世界各地で行われます。本邦でも、開催される地区があるようです。
フローレンス・ナイチンゲールは、クリミア戦争に従軍の後、筋痛性脳脊髄炎/慢性疲労症候群(ME/CFS)にかかっていたのではないかと言われています。彼女は、その後、50年間をほぼ寝たきりの状態だったとも言われています。
そのような彼女にちなみ、看護の日と同じ日に、世界啓発デーが開催されることになりました。

線維筋痛症(FM)は、紫のリボン
筋痛性脳脊髄炎/慢性疲労症候群(ME/CFS」は、青のリボン
化学物質過敏症(MCS)は、緑のリボン
で象徴されます。
そのことを踏まえて、
各地で、大きな建造物に対して、紫、青、緑色のライトアップが行われています。

線維筋痛症(FM)対する理解の新たなパラダイム
本邦の最新の慢性疼痛診療ガイドラインによると、
線維筋痛症(fibromyalgia:FM)は、
『身体の広範な部位に、原因不明の慢性疼痛と全身性のこわばりを主徴候とし、随伴症状として多彩な身体症状、神経・精神症状を伴い、いずれの徴候も慢性疼痛と同様に
身体診察や一般的画像検査を含む臨床検査では症状を説明できる異常を見いだせない。』
と定義されています。
さらに、線維筋痛症の痛みは侵害受容性疼痛ではなく、病巣が特定されない神経障害性様の中枢性疼痛とされており、いわゆる痛みの中枢感作が成立し、中枢感作症候群(central sensitization syndrome:CSS)の一つであると記載されています。また内因性の痛みの抑制メカニズムの欠損であるとも考えられています。
つまり、線維筋痛症の痛みは、脊髄や脳の働きの障害が引き起こすものであるということです。
さらに、近年、線維筋痛症は、侵害受容性疼痛、神経障害性疼痛に次ぐ、第3の痛みとして痛覚変調性疼痛(nociplastic pain)であると明言されるようになりました。
痛覚変調性疼痛(nociplastic pain)とは、末梢侵害受容器の活性化を引き起こす、実質的または切迫した組織障害の明確な証拠がないにも関わらず、
あるいは、痛みを引き起こす体性感覚系に疾患や病変の証拠がないにもかかわらず、侵害受容が変化することによって生じる痛みと定義されています。
本邦における、2022年の線維筋痛症(FM)ついての論文によると、FMは中枢感作症候群(central sensitization syndrome:CSS)の一つであり、痛覚変調性疼痛(nociplastic pain)の代表的疾患であると述べています。
慢性疼痛診療ガイドライン作成ワーキンググループ編: 慢性疼痛診療ガイドライン. 真興交易(株)医書出版部, 東京, 2021
松本美富士:線維筋痛症の臨床:痛覚変調性疼痛とその治療. 現代医学69(1): 44-49, 2022
臼井千恵:線維筋痛症. 臨床精神薬理 25: 513-519, 2022
三木健司:線維筋痛症はどんな病気なの?どうすればいいの?どう支えていく?. 難病と在宅ケア 28(6): 38-42, 2022
ところが…
2013年に1か月違いで、線維筋痛症臨床における革新的な2つの論文が報告されました。
最初に報告された論文は、ドイツのヴュルツブルク大学の 神経学教授であるヌルカン・ユセイラー(Nurcan Üceyler)らによるもの、
次に報告された論文は、米国ハーバード・メディカルスクール・マサチューセッツ総合病院、神経内科医教授であるアン・ルイーズ・オークランダー(Anne Louise Oaklander)らによるものでした。
それによると、線維筋痛症(FM)の一部は小径線維ニューロパチー(small fiber neuropathy:SFN)であり、原因は不明ではなく、一部のFMはSFNとして病理学的に明らかに証明できるものであると述べました。
この報告以来、欧米の線維筋痛症(FM)に対する理解に、SFNの病理が加わり、議論の的となりました。
以後、同様の報告が、数多くなされるようになりました。
・Üceyler N, Zeller D, Kahn AK, et al: Small fibre pathology in patients with fibromyalgia syndrome. Brain 136(6): 1857-1867, 2013
・Oaklander AL, Herzog ZD, Downs H et al: Objective evidence that small-fiber polyneuropathy underlies some illnesses currently labeled as fibromyalgia, Pain 154(11): 2310-2316, 2013

中枢性感作症候群(痛覚変調性疼痛) VS 小径線維ニューロパチー
欧米のFM臨床の世界では、FMの病態理解に対する、中枢性感作症候群(CSS)と小径線維ニューロパチー(SFN)の関連についての議論が多数あります。
実際、由緒ある米国の医学雑誌「PAIN(ペイン)」において、
2015年、ミシガン大学アナーバー校慢性疼痛および疲労研究センター、麻酔学・リウマチ学・精神医学の教授および所長であるダニエル・ジェイ・クロウ(Daniel J Clauw)は、その誌上で、小径線維ニューロパチー(SFN)の報告に対して「小径線維ニューロパチーが線維筋痛症の痛みの〝原因〟であるという考えにうんざりしている」と意見を述べ、さらに「中枢性感作が主要な病態であるという圧倒的な証拠がある」とも述べています。
Clauw DJ: What is the meaning of “small fiber neuropathy” in fibromyalgia? Pain 156(11): 2115-2116, 2015
2016年、その論文に対して、アン・ルイーズ・オークランダー(Anne Louise Oaklander)は、次の年の雑誌「PAIN(ペイン)」上で、「脳の可塑性が関与することには同意する。しかし、中枢性感作が主要な病態である可能性は低い。」と反論しています。
Oaklander AL: What is the meaning of “small-fiber polyneuropathy” in fibromyalgia? An alternate answer. Pain 157(6): 1366-1367, 2016

主張1
SFNとFMの間で多様なケラチノサイト(角化細胞:皮膚の最外層の表皮に存在する主要な細胞であり、ヒトでは表皮の細胞の90%を占める)のトランスクリプトーム(mRNAの総称)・ シグネチャー(2群間を分類する際に使用される特徴的な遺伝子)が得られており、両者の小径線維感受性の病理メカニズムが異なることを示唆し、高度診断の基礎となることが期待される。
Karla F, Bischlerb T, Egenolfa N et al: Fibromyalgia vs small fiber neuropathy: diverse keratinocyte transcriptome signature. Pain 162(10): 2569-2677, 2021
主張2
線維筋痛症(FM)の中枢メカニズムの1つとして同定されている島における興奮性神経伝達物質(グルタミン酸)の増加との関連性が示唆されており、表皮内小径線維密度(IENFD)を減少させる可能性がある。つまり、中枢神経系の変調がSFNにつながる可能性がある。
Harte SE, Clauw DJ, Hayes JM, et al. Reduced intraepidermal nerve fiber density after a sustained increase in insular glutamate: a proof-of-concept study examining the pathogenesis of small fiber pathology in fibromyalgia. PAIN Rep 2: e590.,2017
主張3
病理学的に証明された小径線維ニューロパチー(SFN)患者の大脳辺縁系および疼痛処理領域において、構造的および機能的な障害が確認された。脳形態計測とfMRIを組み合わせることによって、SFNのバイオマーカーを得ることができ、疾患の重症度と中枢神経の関与との関連性を客観的に評価することができる。神経障害性疼痛の末梢感作に加えて、皮膚の変性の伴う脳内反応の低下も明らかになり、末梢神経障害による神経障害性疼痛の中枢メカニズムにも光が当てられた。
Hsieh PC, Tseng MT, Chao CC, et al: Imaging signatures of altered brain responses in small-fiber neuropathy: reduced functional connectivity of the limbic system after peripheral nerve degeneration. Pain 156(5): 904-916, 2015
主張4
線維筋痛症(FM)と診断された患者のうち、小径線維ニューロパチー(SFN)が確認された患者とされなかった患者では、ほとんどの症状が同程度の重症度で認められ、これらの集団が重複していることがさらに証明された。また、いくつかの症状、すなわち、知覚異常の存在と重症度、末梢性自律神経障害の集合的な症状は、症状のある患者間のスクリーニングに予測的な有用性を持つかもしれない。さらなる努力が必要である。
Lodahla M , Treisterb R, OaklanderaAL: Specific symptoms may discriminate between fibromyalgia patients with vs without objective test evidence of small-fiber polyneuropathy. Pain reports 3: 1-6, 2018
主張5
線維筋痛症患者の大きなサブグループに小径線維ニューロパチーが認められたことは、自律神経失調症神経障害仮説を補強し、線維筋痛症の痛みを検証するものである。これらの新しい知見は、線維筋痛症が主として神経学的なものであることを支持するものである。
Lavín M: Fibromyalgia and small fiber neuropathy: the plot thickens!. Clinical Rheumatology37: 3167–3171, 2018
主張6
線維筋痛症(FM)患者における小径線維ニューロパチー(SFN)が確認されたことにより、治療、特に神経障害性疼痛の治療において何らかの示唆を与えることが期待される。これまでFMは、病態生理のはっきりしない曖昧な疾患として扱われ、その診断も主観的な基準に基づいて行われてきた。FMにおけるSFNの研究は強固であり、一部の患者では末梢組織病変の基本的な要素があることが示唆されている。さらに、SFNはFM患者において容易に検出され、診断をより客観的なものにする。さらに、FM で見られる症状の多くは、免疫介在性である可能性が高いという結論に至る。残念ながら、この研究は一部の患者にしか適用できず、FMやSFNが持つ複雑性のすべての側面を説明するためには、まだまだ研究が必要である。
Swiecka M, Maslinska M , Kwiatkowska B: Small fiber neuropathy as a part of fibromyalgia or a separate diagnosis? .Int. J. Clin. Rheumatol 13(6): 353-359, 2018)
主張7
線維筋痛症の診断基準の改訂により、かえって線維筋痛症とSFNを区別することはできない。線維筋痛症とSFNを区別するためには皮膚生検、レーザー誘発電位、QST、角膜共焦点顕微鏡を行うとよい。正しい診断ができれば、患者に適切な情報を提供することができ、薬物療法や非薬物療法を適応させることができる。患者のケアを向上させるために、これら2つの疾患の個別化に関するさらなる研究が必要である。
Bailly F: The challenge of differentiating fibromyalgia from small-fiber neuropathy in clinical practice. Joint Bone Spine 88, 2021
主張8
線維筋痛症(FM)は小径線維ニューロパチー(SFN)と中枢性感作症候群(CSS)の複雑な相互作用による幅広い表現型をもつ疾患である。
de Tommaso, Vecchio E, Nolano M: The puzzle of fibromyalgia between central sensitization syndrome and small fiber neuropathy: a narrative review on neurophysiological and morphological evidence. Neurological Science 43. 1667-1684, 2022
主張9
線維筋痛症(FM)のある症例では中枢神経を介したプロセスが、他の症例では末梢神経を介したプロセスが原因であり、おそらくは、その2つの組み合わせである可能性がある。
Kelley MA, Hackshaw KV: Intraepidermal Nerve Fiber Density as Measured by Skin Punch Biopsy as a Marker for Small Fiber Neuropathy: Application in Patients with Fibromyalgia
私案・一次性(SFNは含む)線維筋痛症(FM)のタイプ
欧米の線維筋痛症(FM)の病態(痛覚変調性疼痛nociplastic pain: NP、小径線維ニューロパチーsmall fiber neuropathy: SFN、虚血性筋痛ischemic myalgia: IM)に対する主張や議論および、本邦における主に永田勝太郎らが報告してきた過去の現象論的臨床仮説に基づく臨床報告を総合して、以下のような、線維筋痛症(FM)の病態に対する私案を創りました。
小径線維ニューロパチー(SFN)型は痛みの表現型が先天性もしくは後天性の感覚神経(Aδ線維とC線維)中心の神経障害性疼痛であり、虚血性筋痛(IM)型は、神経原性(後天性の主にC線維である心血管系自律神経系障害:SFN、先天性・自律神経機能の脆弱性)と筋原性(後天性の心筋代謝障害:栄養障害など、先天性の心筋機能の脆弱性:小心臓症など)により引き起こされるものとしました。
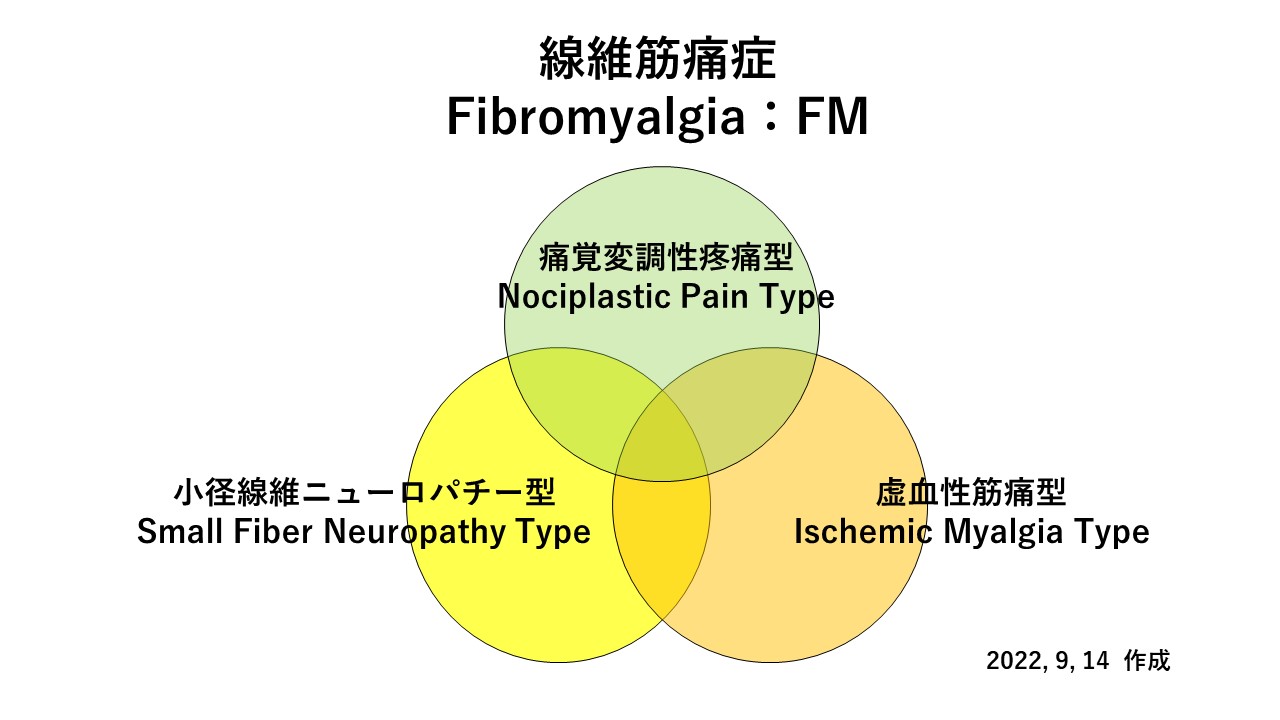
あくまでも現時点での私案です。あくまでも、現時点での線維筋痛症(FM)の患者さんに対する、自分の認知様式を整理するためです。自分自身でも、絶対的なものとして信じていません。当然、世の中のコンセンサスは得られていません。(独善と言えます。)自らの臨床において現象論的態度で検証し、時には創りなおし、すべてを否定し(unlearn:学びほぐし)、時には新たな理論に一新し、再構築し(relearn)、自分自身の線維筋痛症(FM)臨床の参考にしていきたいと思います。


【線維筋痛症(FM)克服、改善のための登山ルート】
多くの臨床家は、中枢性感作症候群(CSS)・痛覚変調性疼痛(NP)の登山ルートを歩いています。
永田勝太郎らは、40年以上の長い間、虚血性筋痛(IM)の登山ルートを歩いてきました。
総合内科医であり、身体的、心理的、社会的医療モデル(bio・psycho・social medical model:BPSモデル)を心身2元論的に歪めて解釈するのではなく、このモデルの提唱者であるDay S、Engel G が理論的基盤としたvon Bertalanffyの一般システム理論に基づくシステム論を中心(心理主義、中枢神経主義ではなく)に臨床を行う心療内科医だからこそ気づいた、線維筋痛症などの慢性疼痛の病態であると考えます。
そして、新たなルートとして、神経内科的病態である、小径線維ニューロパチー(SFN)が見つかりました。
虚血性筋痛(IM)の登山ルートと小径線維ニューロパチー(SFN)のルートは合流したように思います。
線維筋痛症の山(臨床)は、誰も到達していない険しい山であり、困難なMissionです。
もしかしたら、この3つの登山ルートは合流して大きな1本の道になるかもしれません。(あくまでも私見です。)
線維筋痛症(FM)おける虚血性筋痛(IM)のメカニズム

神経障害性微小血管障害(neuropathic microvasculopathy)
SFNによる神経障害性微小血管障害(neuropathic microvasculopathy)により虚血性筋痛(ishemic myalgia:IM)が出現します。
下の3つの項目で、このことを説明いたします。
Oaklander AL, Nolano M: Scientific Advances in and Clinical Approaches to Small-Fiber Polyneuropathy: A Review. JAMA Neurol.76(10): 1240-1251, 2019
1,Albrechtらの報告
2,Doriらの報告
3,心機能への影響
Albrecht PJ, Hou Q, Argoff CE, et al: Excessive Peptidergic Sensory Innervation of Cutaneous Arteriole-Venule Shunt(AVS) in the Palmer Glabrous Skin of Fibromyalgia Patient: Implications for Widespread Deep Tissue Pain and Fatigue.
Dori A, Lopate G, Keeling R, et al: Myovascular innervation: axon loss in small-fiber neuropathies.Muscle & Nerve: 514-521, 2015
1,Albrechtらの報告
【動静脈シャント(AVS)とその支配神経】
毛細血管に直前に流れ込む血管を細動脈といいます。通常、細動脈から毛細血管に細胞に酸素や栄養を多く含んだ動脈血を供給します。
毛細血管から出た血液は、静脈血という酸素や栄養の少ない血液となり、細静脈を通り、心臓へ戻っていくルートを通ります。
しかし、体温調整や全身の血流の調整のため、細動脈から直接、細静脈へ流れ込むルートがあり、
このルートを動静脈シャント(arterio-venous shunt:AVS)と言います。
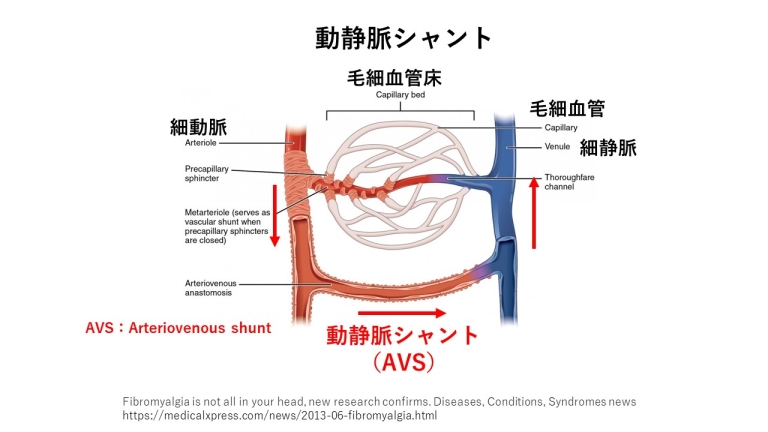
細動脈の血管は、外膜、中膜、内膜に分かれています。
中膜の中に、血管を収縮する役割のある血管平滑筋があります。
血管平滑筋を収縮したり拡張したりする神経は、中膜の血管平滑筋周囲に神経の網(神経叢)を形成し、
そこから神経は平滑筋細胞のすきまに入っていきます。
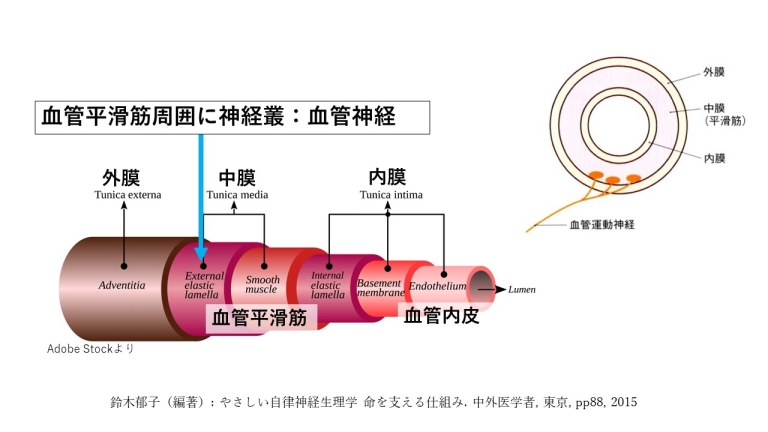
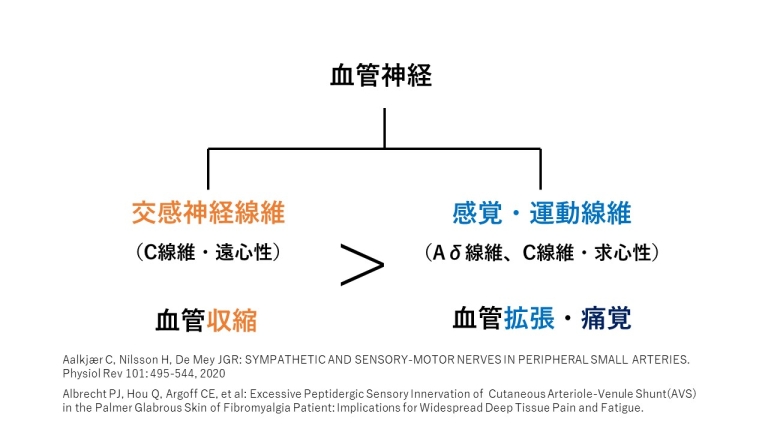
血管神経は2つあります。
1つめは交感神経です。
交感神経は、C線維であり、脊髄から血管へ向かっていく方向へ情報が伝わる遠心性です。そして血管平滑筋に働き、血管を収縮させます。
2つめは、感覚・運動神経です。副交感神経ではありません。
感覚・運動神経は、Aδ線維(少ない)とC線維(多い)で成り立ち、脊髄へ向かっていく方向へ情報が伝わる求心性です。そして血管平滑筋に働き、血管を拡張させます。また、痛みを伝える神経でもあります。
通常は、交感神経は感覚・運動神経より多く存在します。
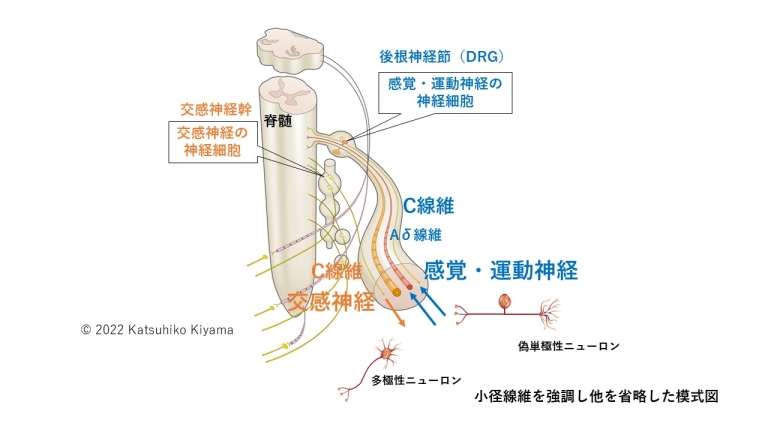
下図の
オレンジの示している、交感神経は主に交感神経幹に神経細胞体があり、血管に向かっています。
青で示している、感覚・運動神経は後根神経節(dorsal root ganglion:DRG)に神経細胞体があり、脊髄に向かっています。
交感神経や感覚・運動神経は、平滑筋のすきまに入り込みます。
神経には膨らんだ部位(膨隆部)が存在します。
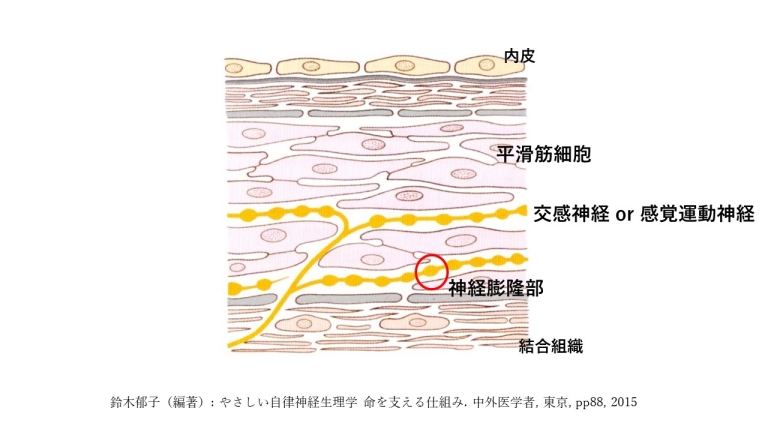
交感神経と感覚・運動神経のそれぞれの神経膨隆部から特有の神経伝達物質が分泌され血管平滑筋に作用します。
交感神経からは、強力な血管収縮物質であるノルエピネフリンやNPY(neuropeptide Y)などが分泌されます。
血管・運動神経からは、強力な血管拡張物資であるCGRP(calcitonin gene-related peptide:カルシトニン遺伝子関連ペプチド)やサブスタンスPなどが分泌されます。
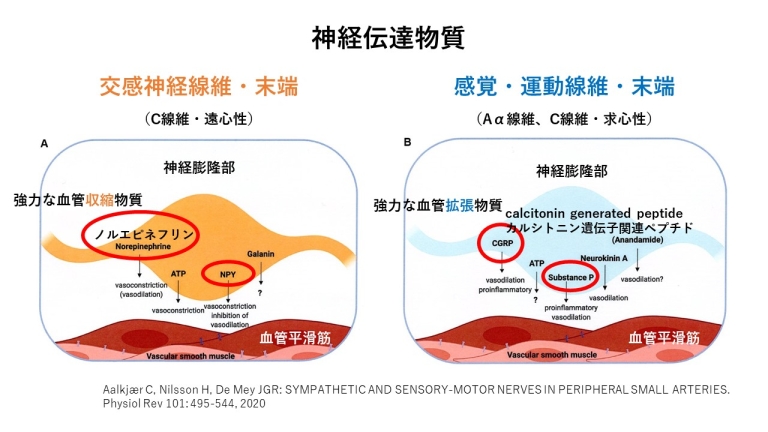
また神経の膨大部には、
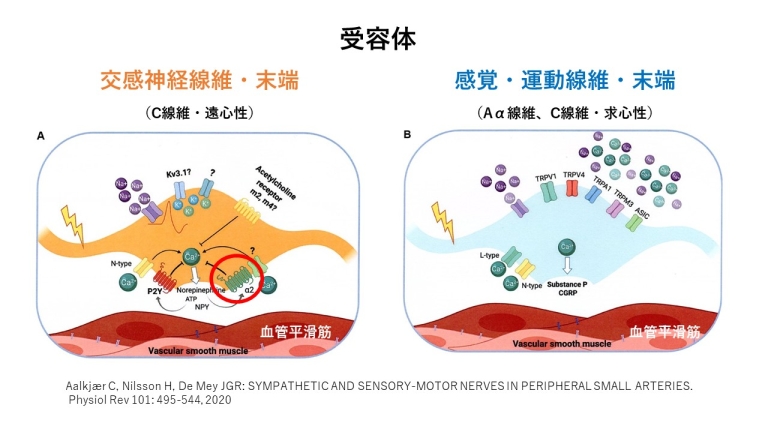
特有の受容体(receptor)があります。
特に、交感神経の膨大部には血管の収縮に関連するα2レセプターが存在します。
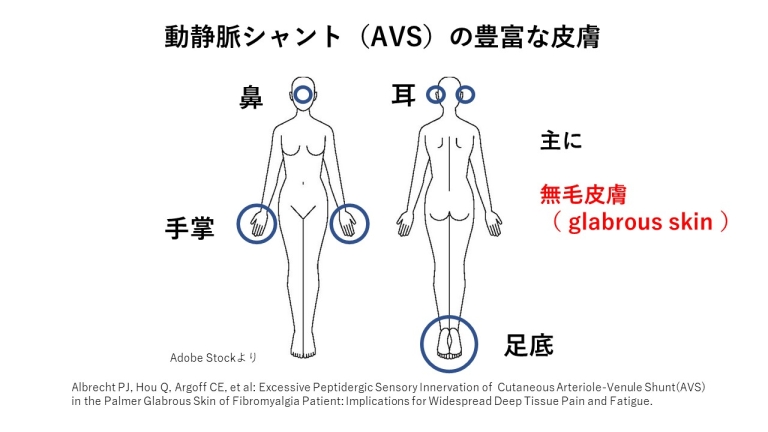
動静脈シャント(AVS)の豊富な部位、
手のひら、足の裏などの毛の生えていない皮膚(無毛皮膚、glabrous skin )に多く分布します。
また、鼻と耳も多い部分です。
ほとんどの、毛ある皮膚(有毛皮膚、hairy skin)には
動静脈シャント(AVシャント)は、手のひらに比べて、はるかに少なく分布します。
また、血管もほとんどありません。
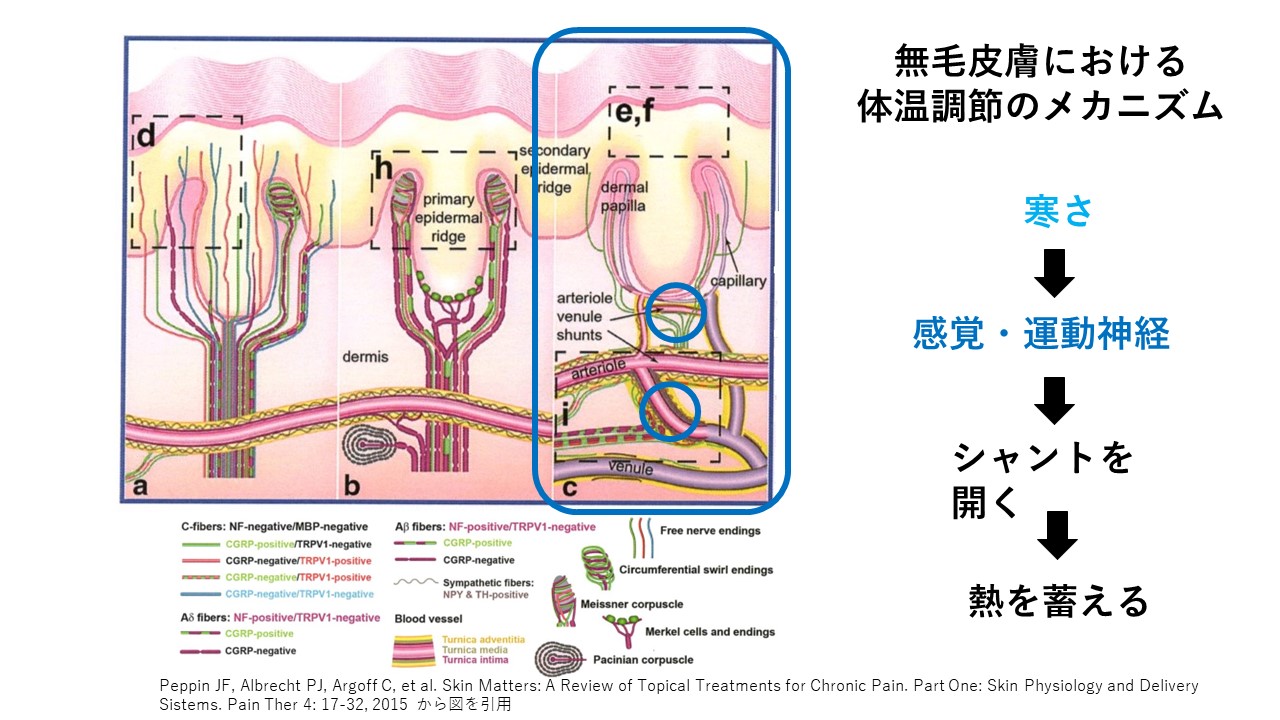
無毛皮膚(grabrous skin)における体温調節を、下図の3枚の図のうち、最も左の図で説明します。
まず、身体に熱さのストレスがかかると、
無毛皮膚(grabrous skin)の交感神経が働き、AVシャント(AVS)を閉じてしまいます。
AVシャントが閉じられると、細動脈の血液の多くは、手のひらの毛細血管に流れ込み、手のひらから熱を放散して身体の熱を下げようとします。

次に、身体に寒さのストレスがかかると、
無毛皮膚(grabrous skin)の感覚・運動神経が働き、AVシャント(AVS)を開きます。
AVシャントが開くと、細動脈の血液の多くは、手のひらには行かず、AVシャント(AVS)を通って、そのまま細静脈に流れ込んで心臓に帰って行きます。
この働きのおかげで、身体の熱を体内に蓄えることができます。
ただし、手のひらは冷たく、時に痛みを感じることになります。
体温調節の働きにおける、血流での調整は、皮膚と骨格筋で行われ、
皮膚と骨格筋の血流は、逆の相関関係にあります。
つまり、皮膚に血流を多くすると、骨格筋の血流は少なく、
皮膚に血流が少ないと、骨格筋の血流は多くなります。
この皮膚と骨格筋の相互作用で体温調整が行われます。
特に、熱ストレスが加わると心拍出量の60%が皮膚に分布し、
手掌の無毛皮膚(grabrous skin):手背の有毛皮膚(hairy skin)は 6:1となります。
つまり、皮膚のうちでも、手のひらや足のうらに身体の多くの血液が流れこむことになります。

【線維筋痛症(FM)患者のAVシャント(AVS)と神経支配】
線維筋痛症(FM)患者のAVシャント(AVS)と神経支配は、正常な人とはずいぶん違っていることが分かりました。
Albrechtらは、AVシャント(AVS)が、最も多く分布している、手のひらの皮膚生検を行った研究を報告しました。
以下が、この結果です。
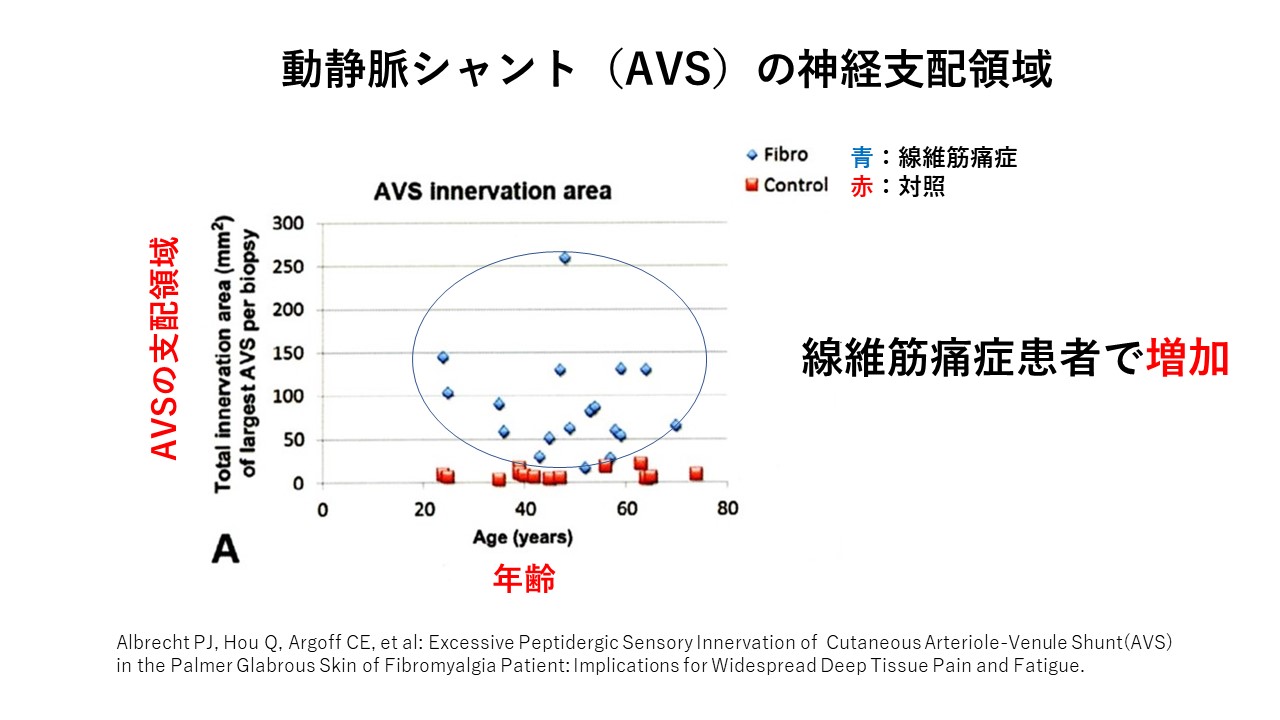
線維筋痛症(FM)患者のAVシャント(AVS)は、正常の人のAVシャント(AVS)より拡大しており、
正常の人の支配神経は交感神経が多いのですが、
線維筋痛症の人は、感覚・運動神経が多くなっていました。

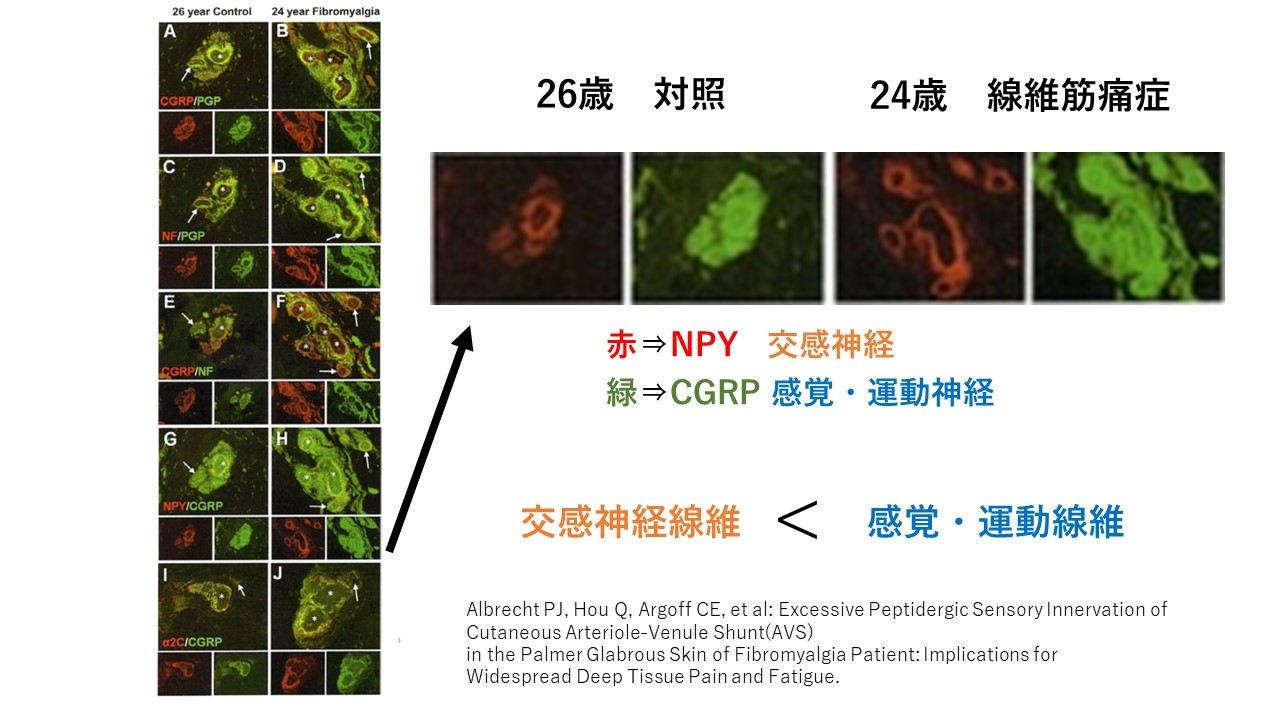
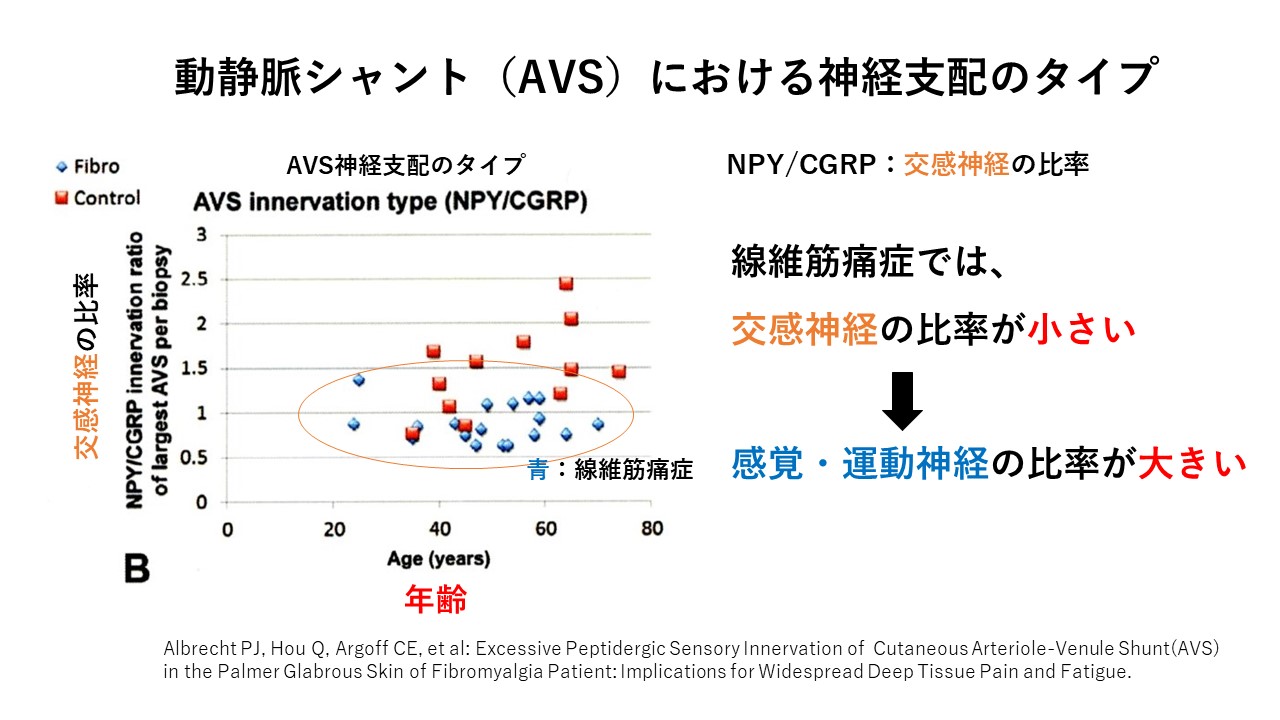
ところが、
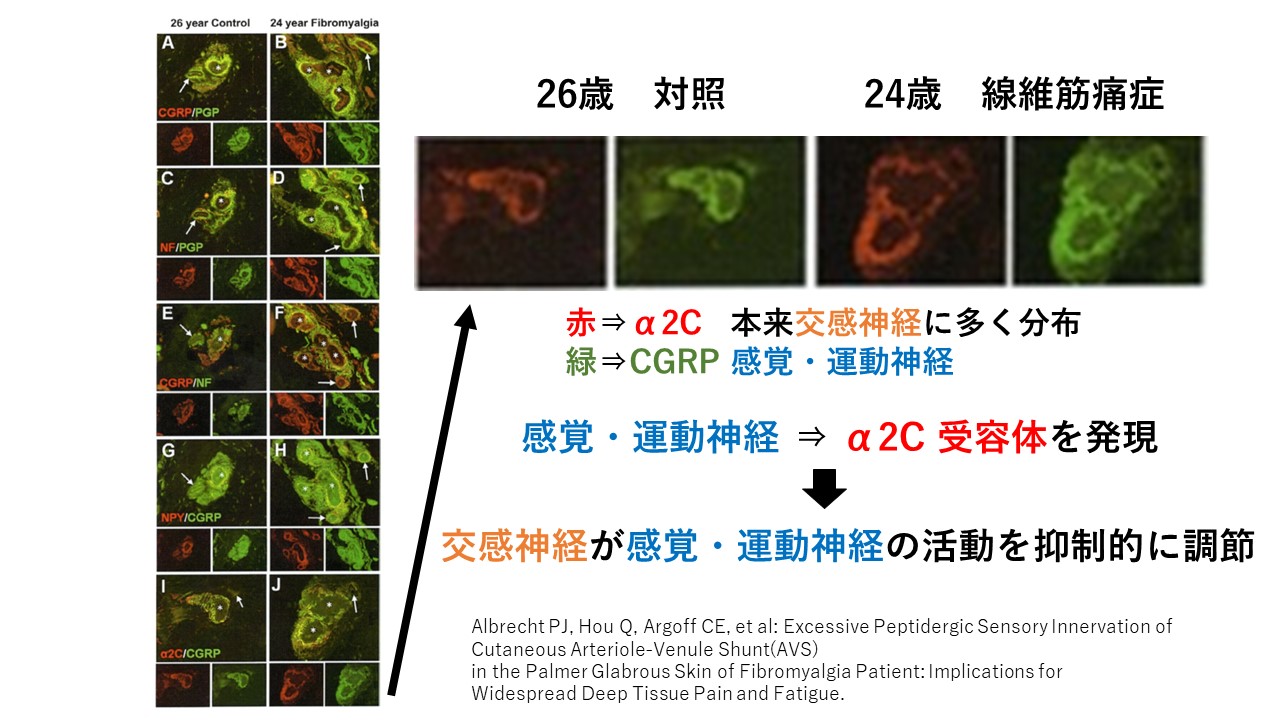
交感神経の受容体であるはずのα2(α2C)受容体が、
線維筋痛症(FM)患者では発現していました。
このことは、交感神経が、感覚・運動神経を抑制しようとする働きを獲得していることが分かります。
線維筋痛症(FM)の発症に抗っているのでしょうか?
正常の人と比べて線維筋痛症(FM)患者は、AVシャント(AVS)の数には変化はありませんでした。
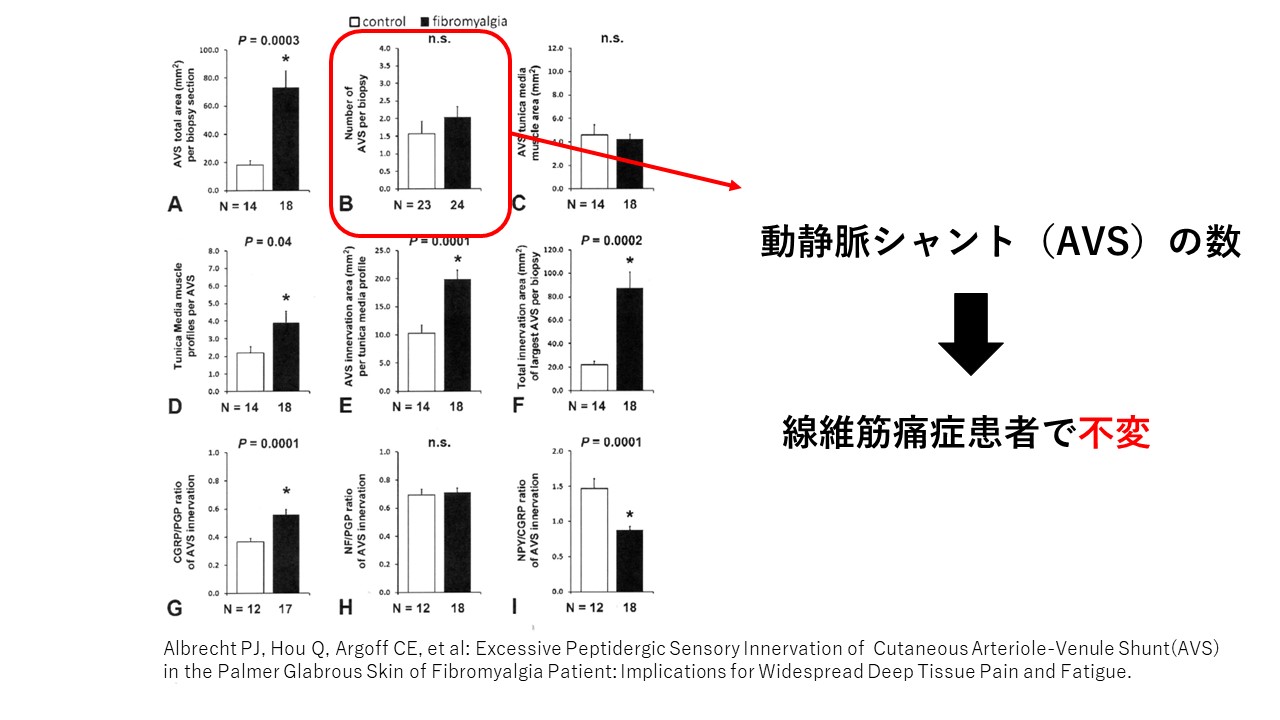
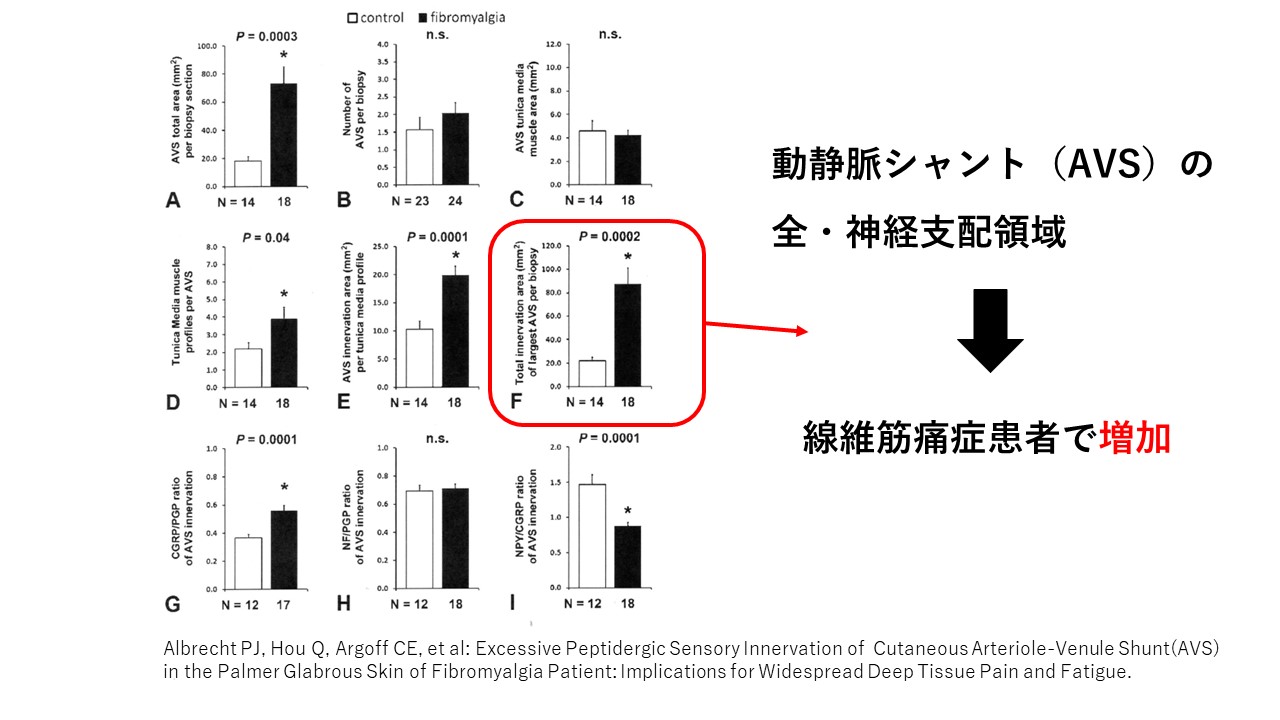
線維筋痛症(FM)患者のAVシャント(AVS)の全神経支配領域は拡大していました。
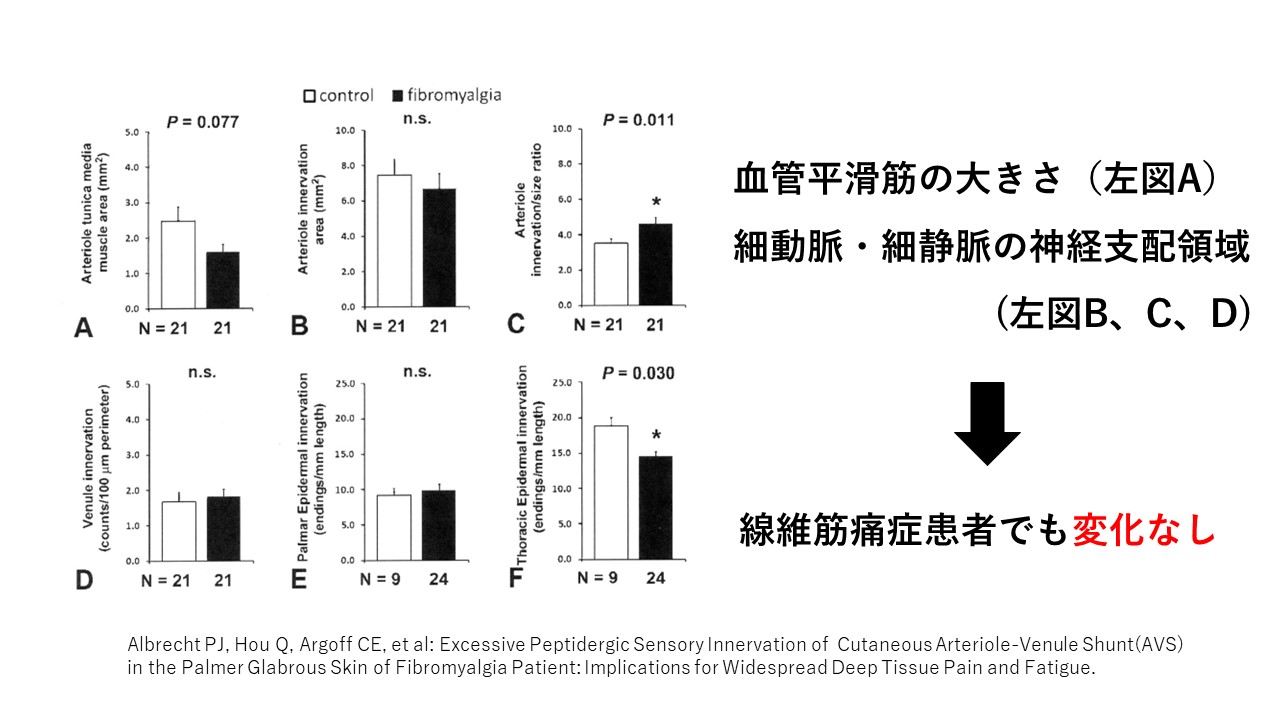
正常の人も線維筋痛症(FM)の人も、血管平滑筋の大きさ、
細動脈および細静脈の神経支配領域に変化はありませんでした。
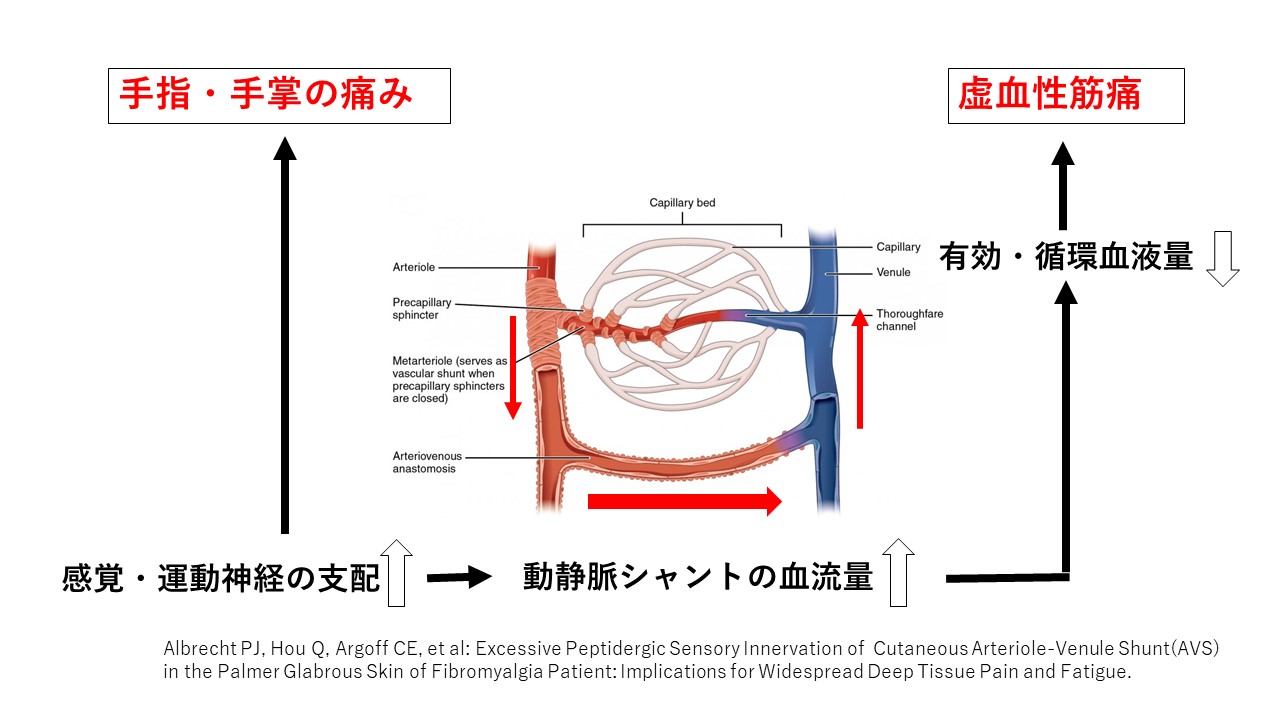
以上のことから
線維筋痛症(FM)患者は、
AVシャント(AVS)が開くことが多くなることになり、
身体の血液の多くを皮膚のシャントの中にため込むことになり、
身体全体を回る血液(有効血液循環量)と骨格筋の血液量が少なくなります。
また、血液て手のひらに届かないため、冷えに弱くなり、感覚・運動神経は痛みの神経でもありますから、
手指に強い痛みを感じるようになります。
ヌルカン・ユセイラー(Nurcan Üceyler)らアン・ルイーズ・オークランダー(Anne Louise Oaklander)らは、
線維筋痛症(FM)患者の表皮内神経線維密度(intraepidermal nerve fiber density :IEFD)、
つまり、皮膚(表皮)の中の、神経線維の数を調べることにより、
線維筋痛症(FM)の一部は小径線維ニューロパチー(SFN)であることを証明しました。
下図のように、線維筋痛症(FM)患者の神経線維は減っています。
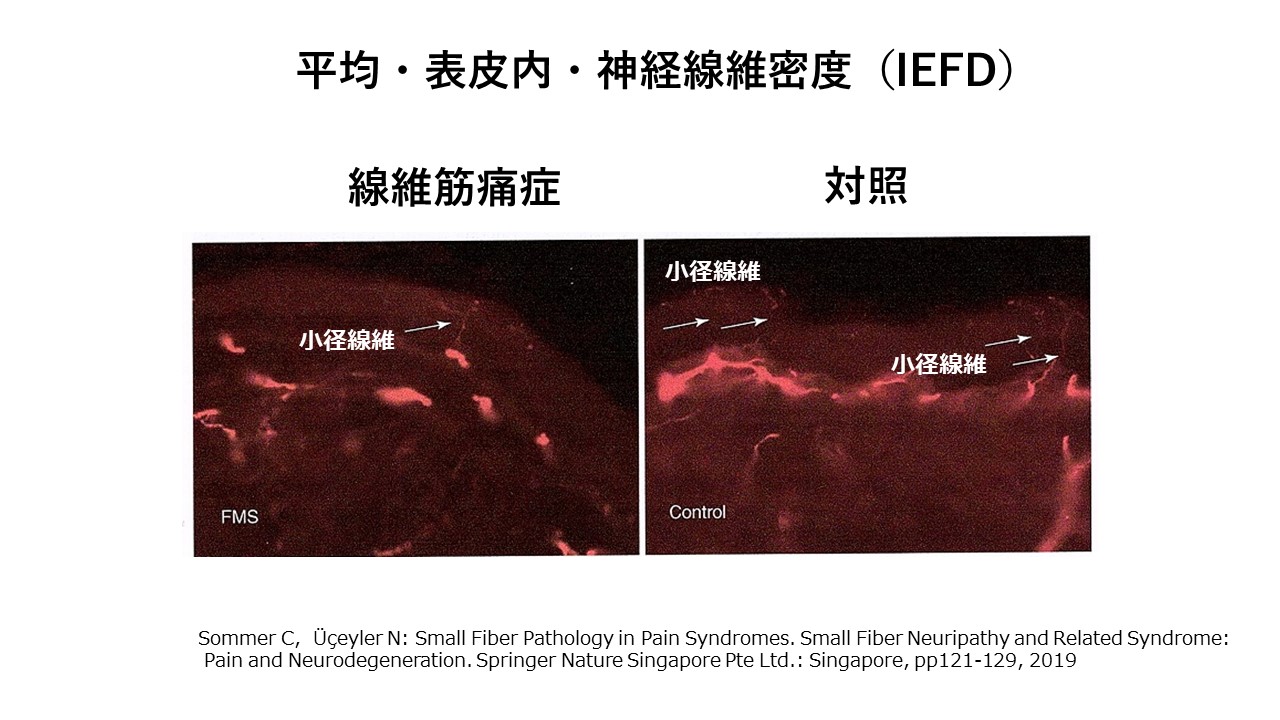
正常の人と線維筋痛症(FM)患者の、平均・表皮内・神経線維密度(IEFD)は、
無毛皮膚(glabrous skin )では、変わらず(有意差なし)、
有毛皮膚(hairy skin)では、明らかに減少していました。(有意差あり)
このことは、平均・表皮内・神経線維密度(IEFD)の低下は、
(圧痛のある)線維筋痛症(FM)の痛みを直接に表現していないと言えます。
つまり、有毛皮膚(hairy skin)の平均・表皮内・神経線維密度(IEFD)の低下が痛みを発しているとは言えないということです。

2,Doriらの報告
【骨格筋の循環と小径線維】
下図は、骨格筋の循環をあらわしています。
右図に、動脈から筋の中に入っていく細動脈が分かります。
左図は、筋の循環の微小循環単位です。
細動脈から筋細胞に酸素や栄養を供給する毛細血管につながっていくことが分かります。
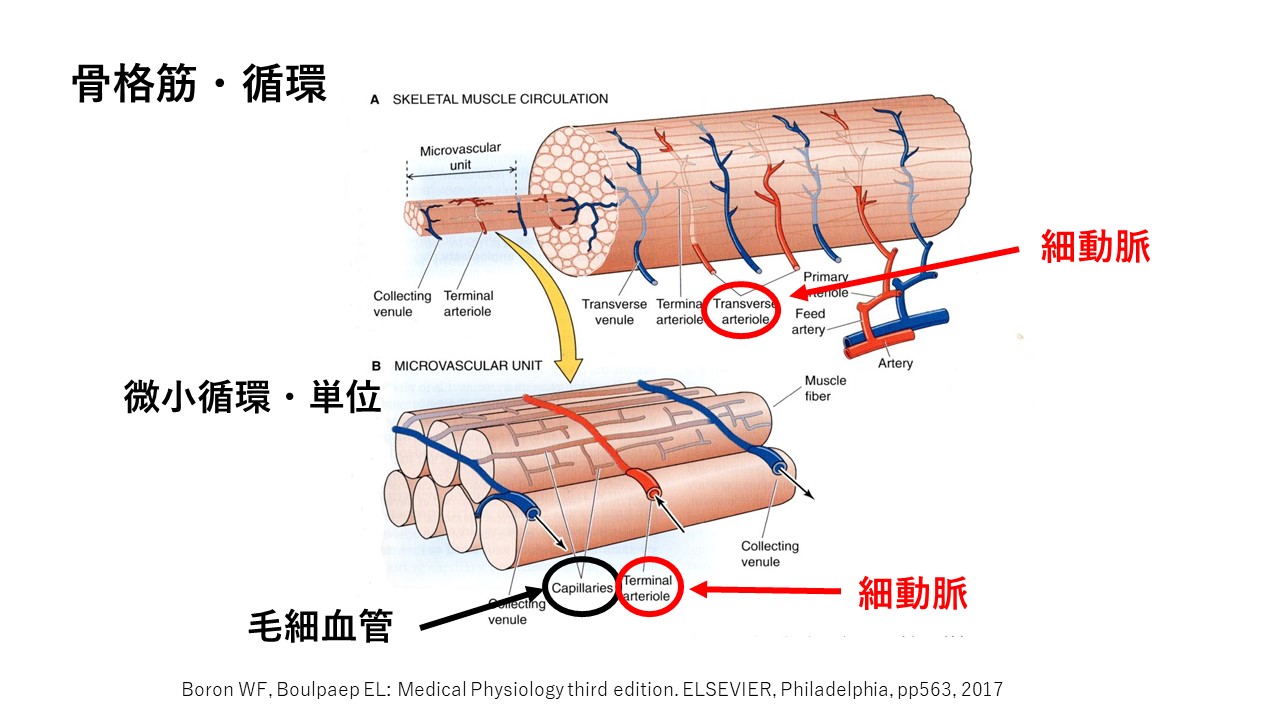
細動脈は、最も神経支配が密になっている動脈です。
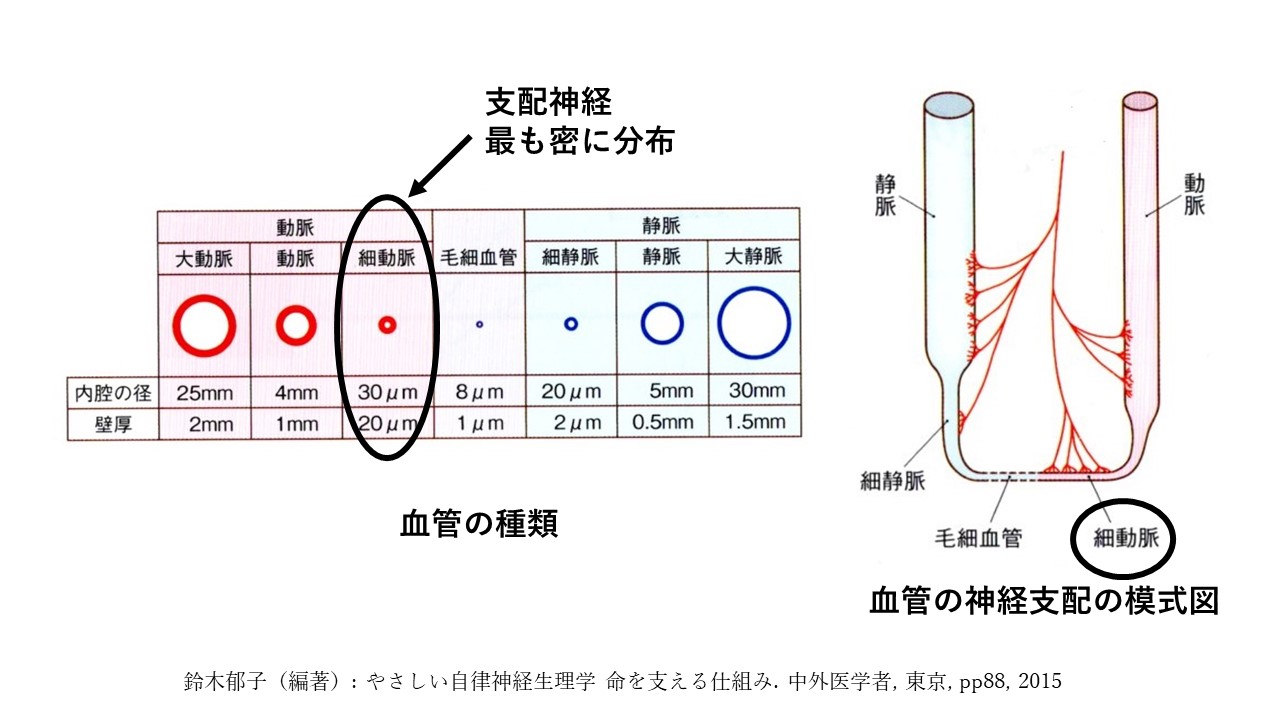
髄鞘化している神経(神経神経)にはAα、Aβ、Aδ線維、B線維があります。
そのうち、Aδ線維は小径線維です。
髄鞘化していない神経(無髄神経)はC線維です。
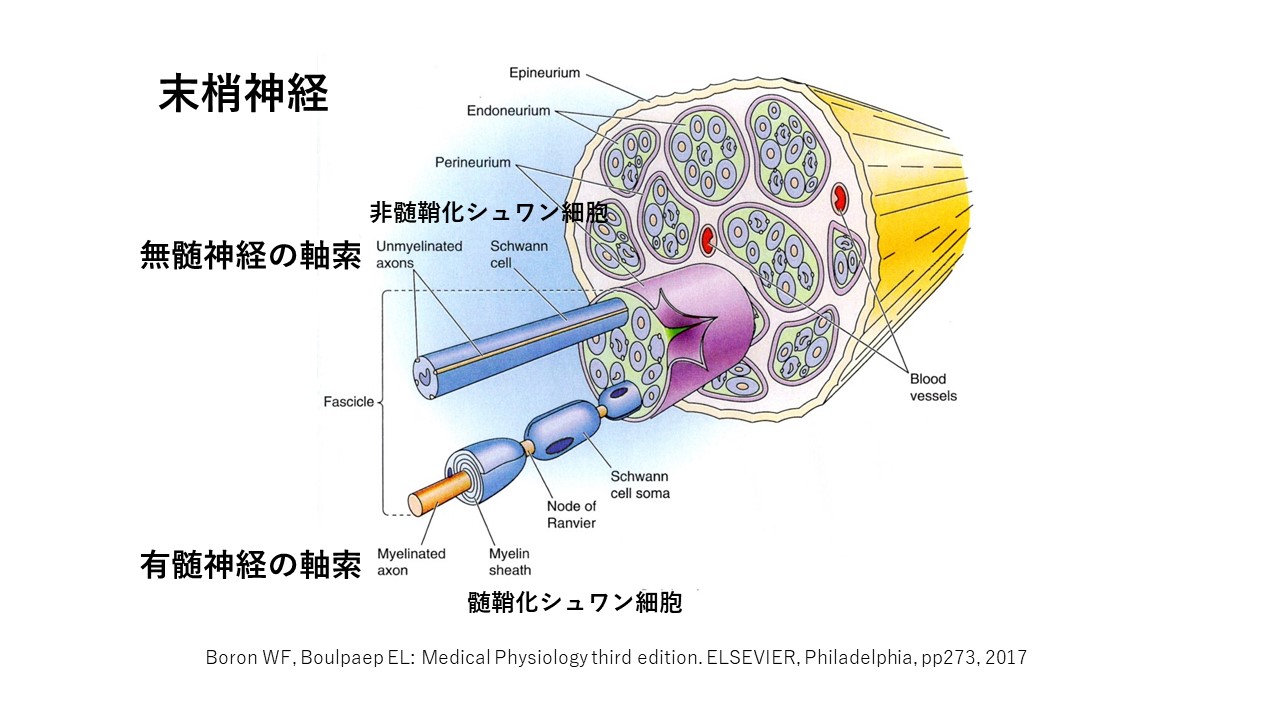
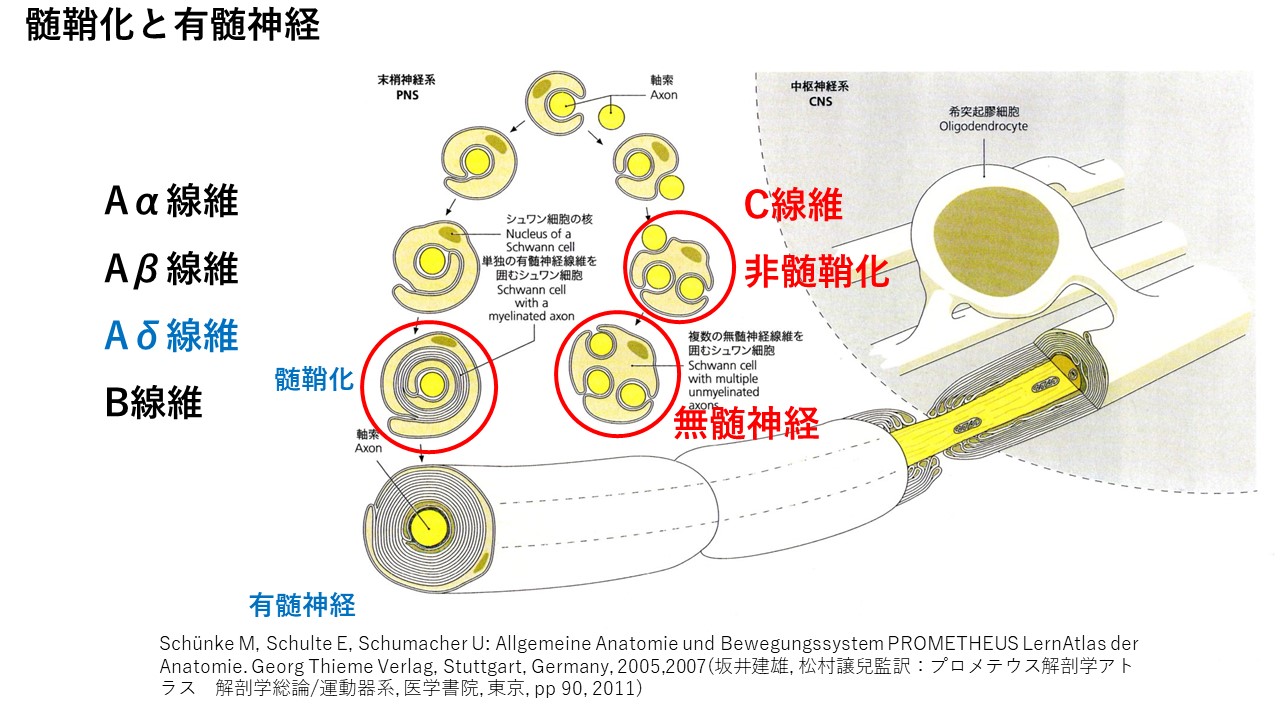
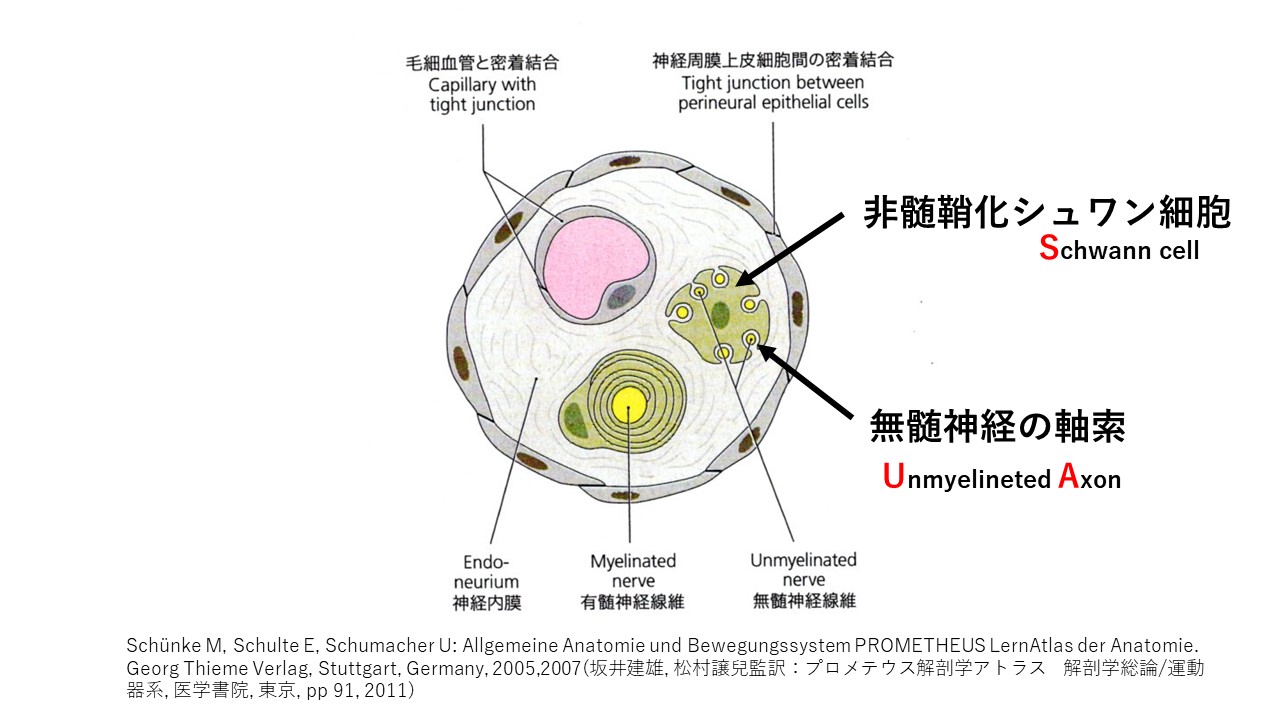
【筋の血管周囲のUAS比についての研究】
UAS比とは、筋の、非髄鞘化(Unmyelineted)の軸索(Axon) と シュワン細胞(Schwann cell)の割合、比のことです。
つまり、非髄鞘化の軸索とは、C線維の軸索であり、
非髄鞘化のシュワン細胞とは、有髄神経のようにバームクーヘンみたいに取り囲んでいるのではなく、
まるでC線維を溝にはめているような入れ物みたいなものです。
この割合がUAS比です。
C線維の軸索が退化してなくなってしまうと、空っぽのシュワン細胞だけが残され、
UAS比は小さくなります。
下図は、正常な人と小径線維ニューロパチー(SFN)患者の、
無髄神経(C線維)と非髄鞘化のシュワン細胞を特殊な方法で染色したも標本です。
小径線維ニューロパチー(SFN)では、
無髄神経(C線維)がなくなっています。
でも、空っぽのシュワン細胞は残っています。
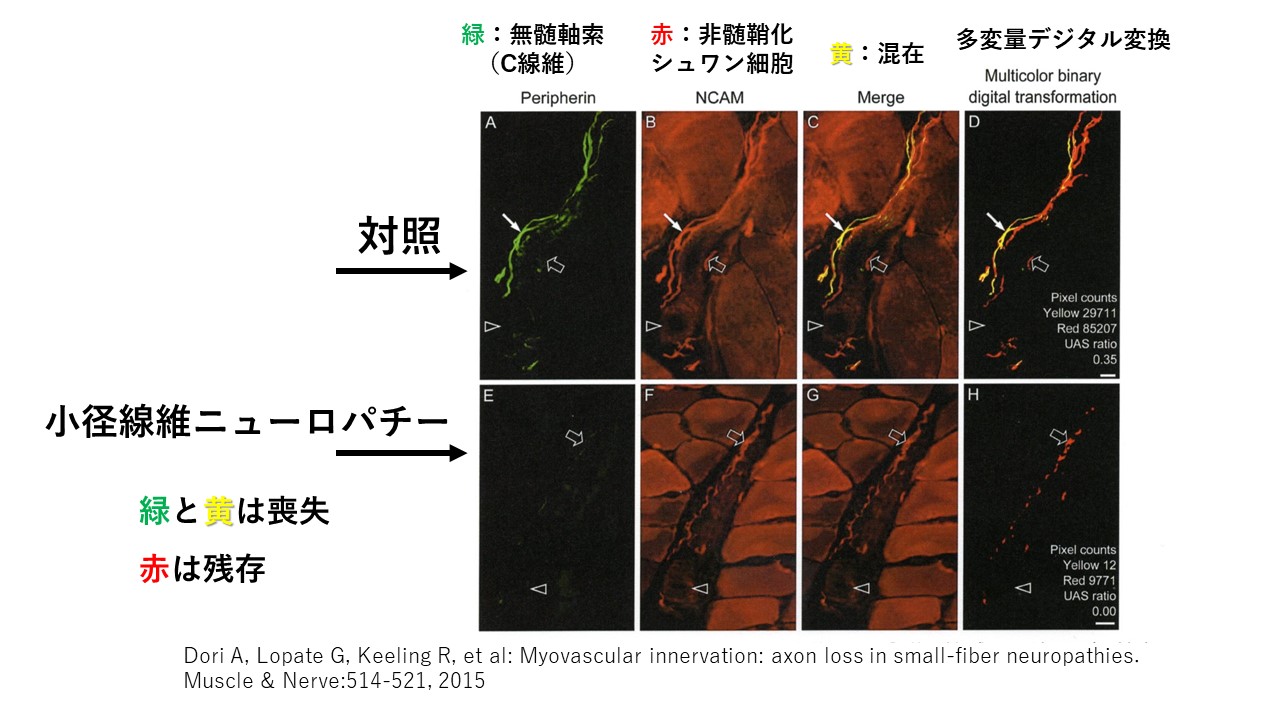
小径線維ニューロパチー(SFN)ではUAS比が明らか(優位)に小さいという結果がでました。

低UAS比(カットオフ値0.25)は小径線維ニューロパチー(SFN)の臨床診断に対して、
感度 90%、特異度 91%という結果でした。
下図は、
AとDが正常の人の、無髄神経(C線維)と非髄鞘化のシュワン細胞です。
軸索は途切れることなく、ほぼ均一の幅で、つながっています。
B、C、Eは小径線維ニューロパチー(SFN)患者のものです。
軸索はビーズ状であり、不規則なシュワン突起が観られます。
シュワン細胞が空っぽであることに由来します。

その他の研究結果は以下のとおりです。
低UAS比(0.25)の患者は、自律神経系の異常が63%、
正常UAS比の患者は、自律神経系の異常が0%であった。
低UAS比(0.25)の患者は、長さもしくは非長さ依存性の疼痛、温度感覚の喪失が19人中10人、
正常UAS比の患者は、長さもしくは非長さ依存性の疼痛、温度感覚の喪失が12人中2人であった。
下肢皮膚の平均・表皮内・神経線維密度(IEFD)と筋の血管周囲のUAS比は、相関がありました。

3,心臓機能への影響
線維筋痛症(FM)における小径線維ニューロパチー(SFN)により起きる虚血性筋痛(IM)は以下にまとめられます。

2022年、線維筋痛症の45%は自律神経性・小径線維ニューロパチーであるとのメタ解析が報告されました。
それは、心拍変動、ヘッドアップチルト試験、定量的発汗性軸索反射(QSART)、皮膚電気コンダクタンス、交感神経皮膚反応、レーザー・ドップラーなどの検査による研究方向でした。
Galosi E, Truini A, Di Stefano G: A systematic Review and Meta-Analysis of the Prevalence of Small Fibre Impairment in Patients with Fibromyalgia. Diagnostic 12, 2022
Levine Tの分類では以下になります。
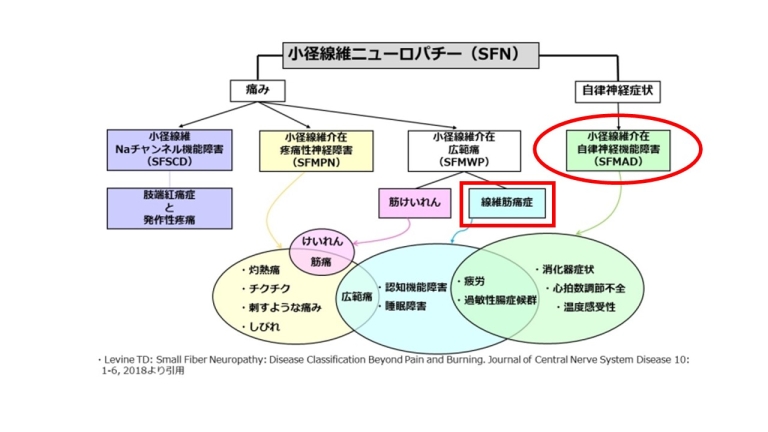
下図のように、心臓の変力作用(inotropic action)に影響するのは、小径線維ニューロパチー(SFN)と心筋代謝障害です。
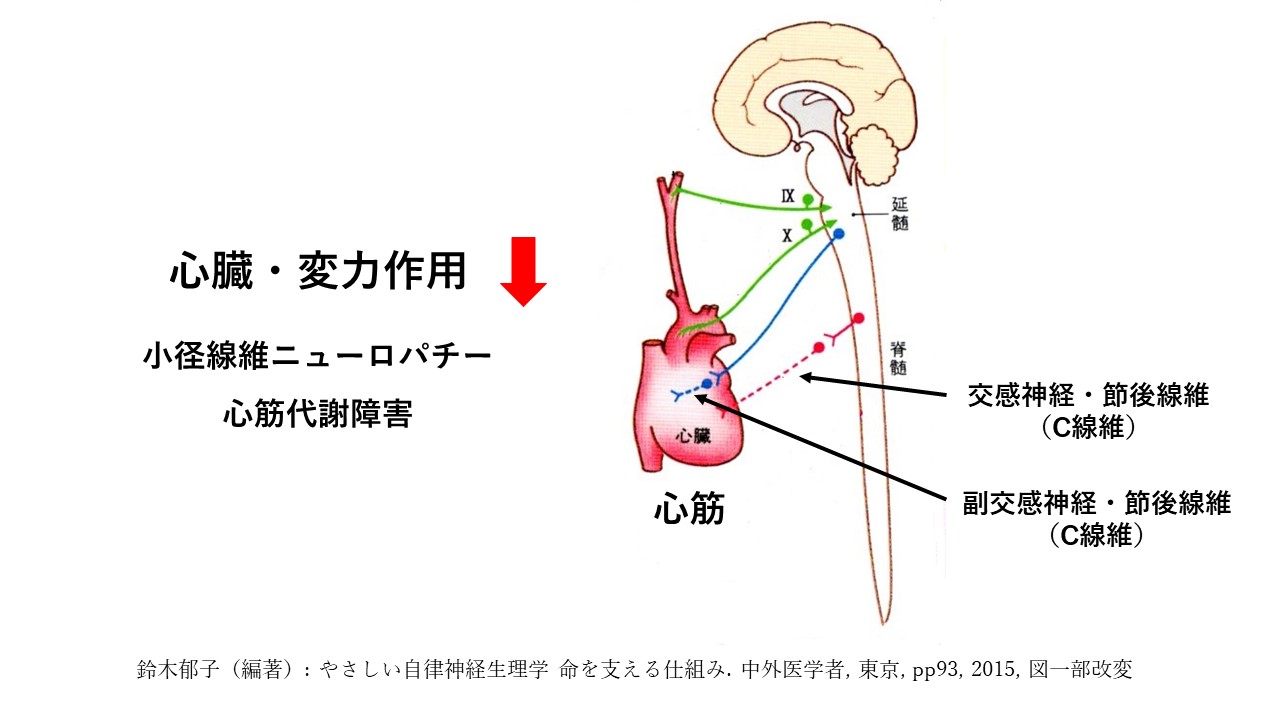
虚血性筋痛(IM)としての線維筋痛症(FM)に対して、小径線維ニューロパチー(SFN)と心筋代謝障害の視点から見ると
下図のようになると考えられます。

Dysdynamische Syndrome
永田勝太郎らは、1980年代より、ヘッドアップ・チルト試験(head-up tilt test: HTT)あるいはシェロングの起立試験(active standing test: AST)に伴う血行動態を、ParamaTec製の血行動態測定器(GP303sなど)を使用することにより、コロトコフ音図から心係数、全末梢血管抵抗などを算出し、病態理解につなげていました。
GP303sは現在、発売中止となっており、当院ではGP nico PS501を使用しています。
その他、血行動態を測定できる機器として、Finapres Medical System社 Finapres NOVAがあります。多くの研究報告はこの機器で行われいます。
Parama Tec社ホームページhttps://www.parama-tech.com/ より・

永田勝太郎らは、長年、この機器を使用して、全身の痛み、慢性の痛みの患者さんの血行動態を測定し、臨床報告を続けてきました。
特に、血行不良タイプ(Dysdynamische Syndrome血行動態不良症候群、hypokinetische Herzsyndrom低反応型:有効循環血液量の低下、心臓のinotropic の低下 ⇒ 心拍出量の低下)が、病態の中心であるとの結果を報告し続けていました。
血行不良タイプでは、起立不耐症、労作不耐症、多彩な症状を引き起こすと考えらます。
線維筋痛症(FM)は末梢病態と中枢病態の相互作用であり、中枢性感作の影響が少ない末梢病態のうちに治療を行わなければならないと考えてきた永田にとって、小径線維ニューロパチー(SFN)の存在は、彼が考えてきた病態のブラックボックス的存在だったと考えられます。慢性疼痛の臨床において、永田はシステム論的思考、患者さんの観察に基づく現象論的思考、臨床結果によりDysdynamische Syndromeの病態概念の必要性を証明してきました。近年、線維筋痛症(FM)小径線維ニューロパチー(SFN)の病理などが明らかになるに従い、Dysdynamische Syndromeの病態を線維筋痛症(FM)の潜在的な病態といち早く認識していた永田の臨床感覚の正当性が証明されたようで、非常に感慨深いことです。
★ParamaTec社GP303s, nico PS 501などの機器で測定した結果を線維筋痛症の病態理解につなげるには、ドイツの循環器心身医学の分野で使用されているDysdynamische Syndrome (血行動態不良症候群)の病態概念は非常に有用でした。
本邦における虚血性筋痛(ischemic myalgia)の理論の歴史
本邦において、永田勝太郎らは、早くから筋細胞への微小循環障害が、全身の痛みや慢性の痛みの大きな要因になる考えていました。そして、心血管系の機能異常が、それを引き起こすと考えていました。そのことは、1987年の論文にすでに発表されていました。そして、全身の痛みや慢性の痛みの脆弱性要因として、小心臓症やDysdynamische Syndrome(起立不耐症)の存在を指摘していました。
永田勝太郎, 村山良介: 慢性疼痛と血行動態 ・血行動態の改善が疼痛の解除につながる. 医学のあゆみ 142(11): 804, 1987
永田勝太郎は、この報告の前に、
九州大学医学部心療内科初代教授を退官し、小倉記念病院の院長であった池見酉次郎先生の元で、
晩年の弟子として心療内科の研修をしていました。
研修をしながら、その当時の自律神経学の大家であった、鳥取の本多和雄先生の元で、教えをいただいており、
この理論の確信を抱いていました。
本多和雄、稲光哲明 編著:起立性低血圧の基礎と臨床. 新興医学出版社, 東京. 2006
永田勝太郎は、起立不耐症の基礎病態となる疾患概念として、ドイツの自律神経学者であるDelius Lらが提唱した循環器心身医学に基づく分類を東京大学心療内科教授の石川 中先生が分かりやすく分類したものを導入しました。以下が石川 中先生が述べた内容です。
1)Dysrhythmische Syndrome:精神心理因子が心拍リズムに影響を及ぼすもの
2)Dysdynamische Syndrome:精神心理因子が循環器系に対し、血行力学的な影響を及ぼすもの
‥‥① hyperkinetische Herzsyndorom:動揺性高血圧、頻脈、軽い収縮期雑音、皮膚温上昇
‥‥② hypokinetische Herzsyndrom:機能性心機能不全(全身倦怠と脱力)
3)Dysathetische Syndrome:心および血管系に異常感覚をもつもの
‥‥‥心臓神経症や四肢末端の血管の異常(AkroparethetischeおよびErythromelalgia)
石川中:循環器の心身症. 心身医学-基礎と臨床-. 朝倉書店, 東京. pp470-478, 1979
永田勝太郎は、この分類のうち、2)Dysdynamische Syndromeに注目し、血行動態不良症候群と名づけました。また、hyperkinetische Herzsyndromを高反応型、 hypokinetische Herzsyndromを低反応型と名づけました。
以後、永田勝太郎らは、全身性の疼痛、慢性の疼痛の基本病理を、主に脆弱性要因およびさまざまなストレッサーにより引き起こされる心血管系の機能異常であるDysdynamische Syndrome(血行動態不良症候群)、hypokinetische Herzsyndrom(低反応型)を中心として臨床報告を次々と行いました。
永田勝太郎: 機能性身体症候群(FSS)としての慢性疼痛-線維筋痛症の臨床から-. 慢性疼痛 32: 25-32, 2013
永田勝太郎: 線維筋痛症の背後に潜む疾患. 慢性疼痛 34: 191-194, 2015
近年では、血行動態不良症候群、低反応型を引き起こす病態として、酸化ストレスおよび糖化ストレスの影響を強調しており、小径線維ニューロパチーの発症病理と一致するようになりました。
永田勝太郎, 志和悟子, 大槻千佳ほか:線維筋痛症の発症要因の追究:糖化, 酸化, 血行動態について. 慢性疼痛 39(1): 114-118, 2020
Dysdynamische Syndrome(血行動態不良症候群)hypokinetische Herzsyndrom(低反応型)は、心原性(心筋代謝障害:栄養障害、酸化ストレス、糖化ストレス、先天性の脆弱性:小心臓症など)および神経原性(小径線維ニューロパチー、先天性の自律神経機能の脆弱性)に分類されるが、ほぼこの2つの混合型です。
喜山克彦, 永田勝太郎: 機能性身体症候群の筋骨格系疼痛に対してホメオスタシスの歪みを中核病理とする意義. 慢性疼痛 40(1): 103-108, 2021
この疾患概念は、起立不耐症を、ストレス負荷による心血管系機能異常の視点(心身医学的視点)から述べたものと考えられます。現在でも、ドイツでは、循環器障害の心身医学的病態としてDysdynamische Syndromeの病名を使用しています。
Jürgen Bの循環器疾患に関する書籍ではDeliusの示した用語が変更されていました。
以下のとおりです。
hyperkinetische Herzsyndrom ⇒ hyperdyname Regulationsstörungen:高動態調節障害
hypokinetische Herzsyndrom ⇒ hypodyname (hypotone) Regulationsstörungen:低動態(低血圧性)調節障害
さらに
normodyname(normotone) Regulationsstörungen:正常動態(正常血圧)調節障害が
分類に追加されています。
Jürgen Barmeyer: Psychovegetative bedingte Hertz-Kreislauf-Strörungen. Das kardiologische Gutachten Anleitungen zur differenzierten Begutachtung bei Hertz-Kreislauf-Erkrankungen. Georg Thieme Verlag, Stuttgart, New York. pp276-285, 2010
虚血性筋痛(IM)と小径線維ニューロパチー(SFN)の病態の接点
心拍出量(心臓が押し出す血液の量)の低下に影響を及ぼす後天的原因には
1,筋原性(心筋代謝障害)
2,神経原性(小径線維ニューロパチー:SFN、心血管系自律神経障害)⇒ 有効循環血液量の減少
が考えられます。
小径線維ニューロパチー(SFN)の発症の原因には、
後天性、遺伝性、症候群性および特発性に分けられます。
約50%は特発性です。
後天性、遺伝性、症候群性の疾患による線維筋痛症(FM)は注意が必要です。
特に、近年の報告では、免疫系の病態による小径線維ニューロパチー(SFN)が注目されています。
特発性小径線維ニューロパチー(idiopathic SFN:iSFN)と心筋代謝障害はほぼ同じ要因、つまりホメオスタシスの歪みで発症すると考えられます。
ホメオスタシスの歪みとして、
糖化ストレス、酸化ストレス、ビタミン不足もしくは過剰などが挙げられます
虚血・再灌流損傷(ischemic-reperfusion injury:IRI)
虚血はほとんどの場合、永続的ではなく、血流は少なくとも部分的に再確立されます。
このことにより、ミトコンドリア機能を損ない、筋線維を損傷し、アポトーシスを促進させる
フリーラジカルおよび過酸化水素のような活性酸素種(ROS)の生成を特徴とする、
複雑な、虚血・再灌流障害(ischemia-reperfusion injury:IRI)が生じます。
さらに、再灌流段階では、筋の微小血管系は、その透過性の増加と損傷へ至り、
損傷組織に活性化したリンパ球が隔離されやすくなります。
主にマクロファージと好中球は、インターロイキン-1(IL-1)や腫瘍壊死因子(tumor necrosis factor:TNF )などの
痛覚促進サイトカインを放出します。
ラジカル酵素を含む細胞内顆粒は、細胞の損傷をさらに増大させ、ひいては障害に対する免疫反応を増大させます。
末梢血流障害における筋痛発生の基本的メカニズムは、虚血・再灌流の長さが関係すると報告されています。
Queme LF, Ross JL, Jankowski MP: Peripheral Mechanisms of Ischemic Myalgia. Front Cell Neurosci 11: 1-15, 2017
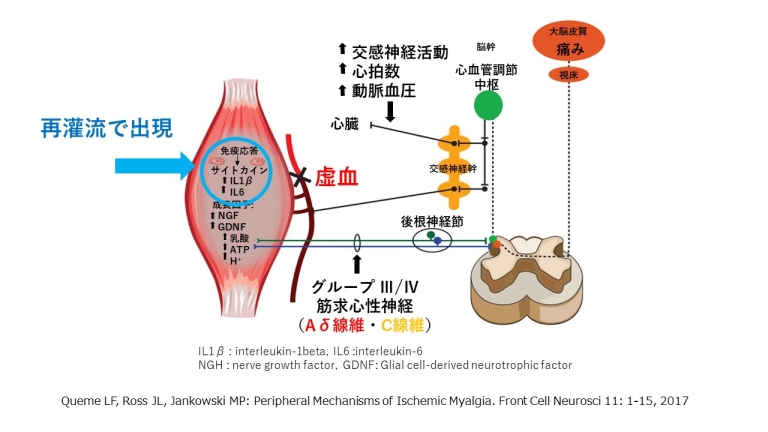
筋の虚血性損傷後の反応
筋求心性神経:Ⅲ・Ⅳ群線維(Aδ・C線維)の反応
虚血性損傷を起こした筋のfascia(間質)にはATP、乳酸、低pH:プロトン(H+)などの代謝産物や過酸化水素など有害なフリーラジカルが発生し、
それらの刺激にⅢ・Ⅳ群線維(Aδ・C線維)が反応します。虚血状態ではⅣ群線維(C線維)が優先的に活性化します。
ATP、乳酸、低pH:プロトン(H+)の3つがそろった時のみ機械的疼痛過敏を誘発することができると報告されています。
Ⅲ群(Aδ線維)の約70%が機械的感受性を持つのに対して、
Ⅳ群(C線維)は約30%が機械的感受性を持ち、60%以上が化学的感受性を有しています。
化学的に敏感な神経ニューロンには、
低代謝物応答(pH7.4-7.0で増加)ニューロンと
高代謝物応答(pH7.0-6.6で増加)ニューロンが存在することが分かりました。
低代謝物応答(pH7.4-7.0で増加)ニューロンは正常時に働く求心性神経のグループで
高代謝物応答(pH7.0-6.6で増加)ニューロンは、虚血性損傷時に生成される代謝物の濃度を感知する求心性神経のグループです。
低代謝物(pH7.4-7.0)の混合物を筋肉内に注射された被験者は筋肉の疲労を訴え、
高代謝物(pH7.0-6.6)の混合物を筋肉内に注射された被験者は筋肉の痛みを感じたと報告されています。
虚血・再灌流損傷(IRI)後には、低代謝物反応性が高まり、後根神経節(DRG)内の
代謝受容体の数が損傷を受けていない対照群に比べて減少していました。
虚血性損傷後の後根神経節(DRG)の構成が切りかわることを示唆しています。
Queme LF, Ross JL, Jankowski MP: Peripheral Mechanisms of Ischemic Myalgia. Front Cell Neurosci 11: 1-15, 2017
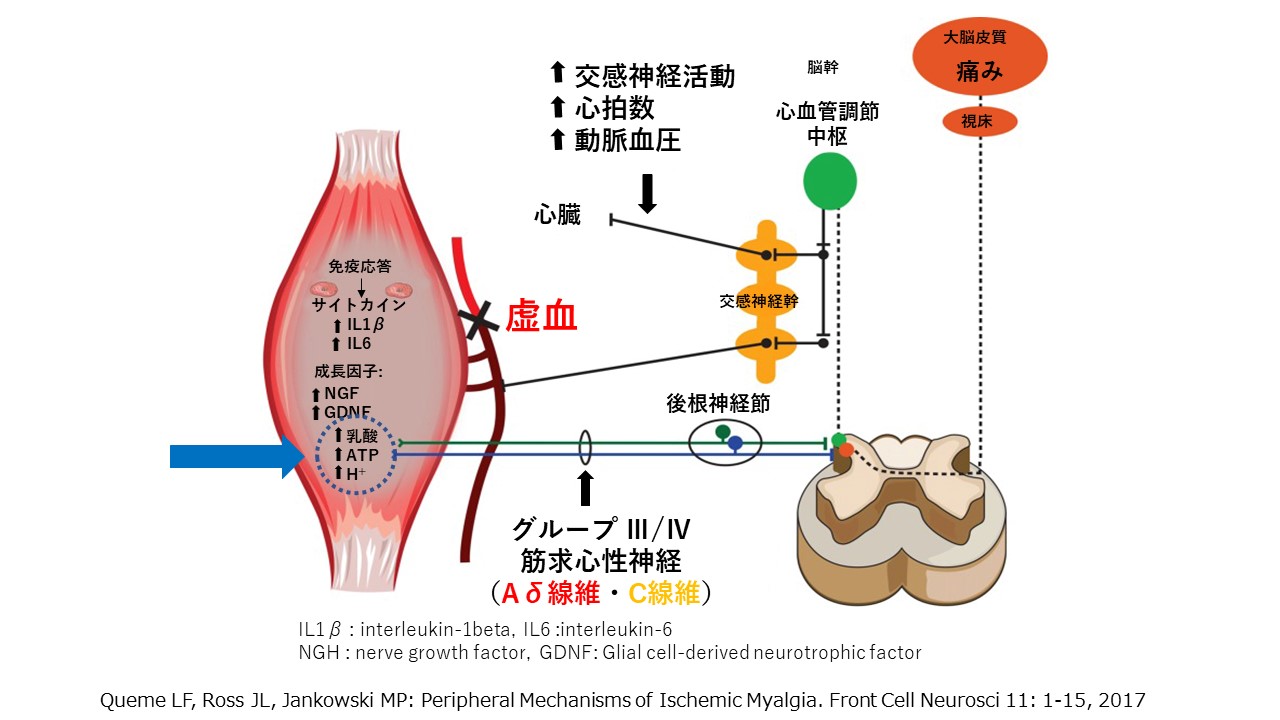
fascia(ファッシア)の痛み
Ⅳ群線維はC線維に相当し、終末の多くはfasciaと骨格筋内の細動脈壁に存在します。
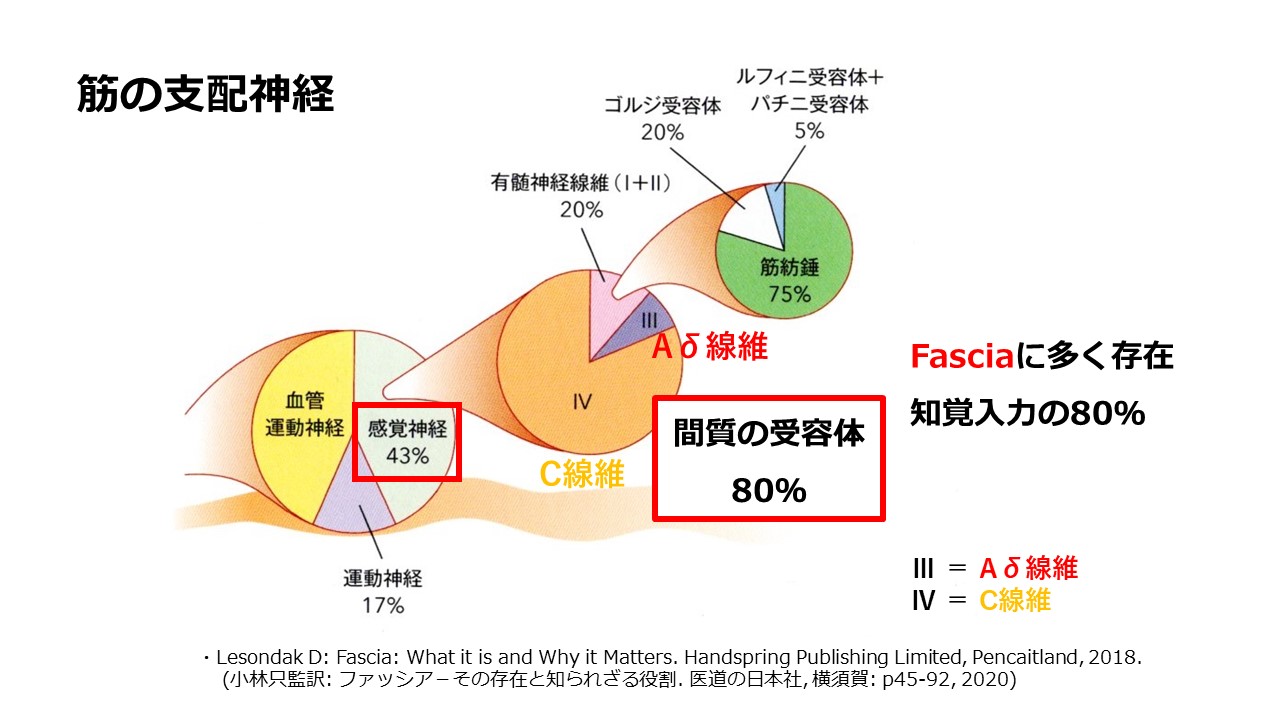
筋の支配神経は
・約43%の感覚神経(Aβ、Aδ、C線維)
・約40%の血管運動神経(交感神経節後線維:C線維、および感覚・運動神経:Aδ線維、C線維)
・約17%の運動神経(Aα、Aβ線維)
で構成されます。
fasciaの感覚神経の約80%は、Ⅲ群線維(Aδ線維)およびⅣ群線維(C線維)であり、
特にⅣ群線維(C線維)が多くを占め、
間質受容体(自由神経終末)としてfasciaに多く存在します。
Fasciaは全身におよぶ連続する広大な一枚の構造を持ち、筋、骨、関節、腱、内臓を覆い最も大きな感覚器官と言われます。

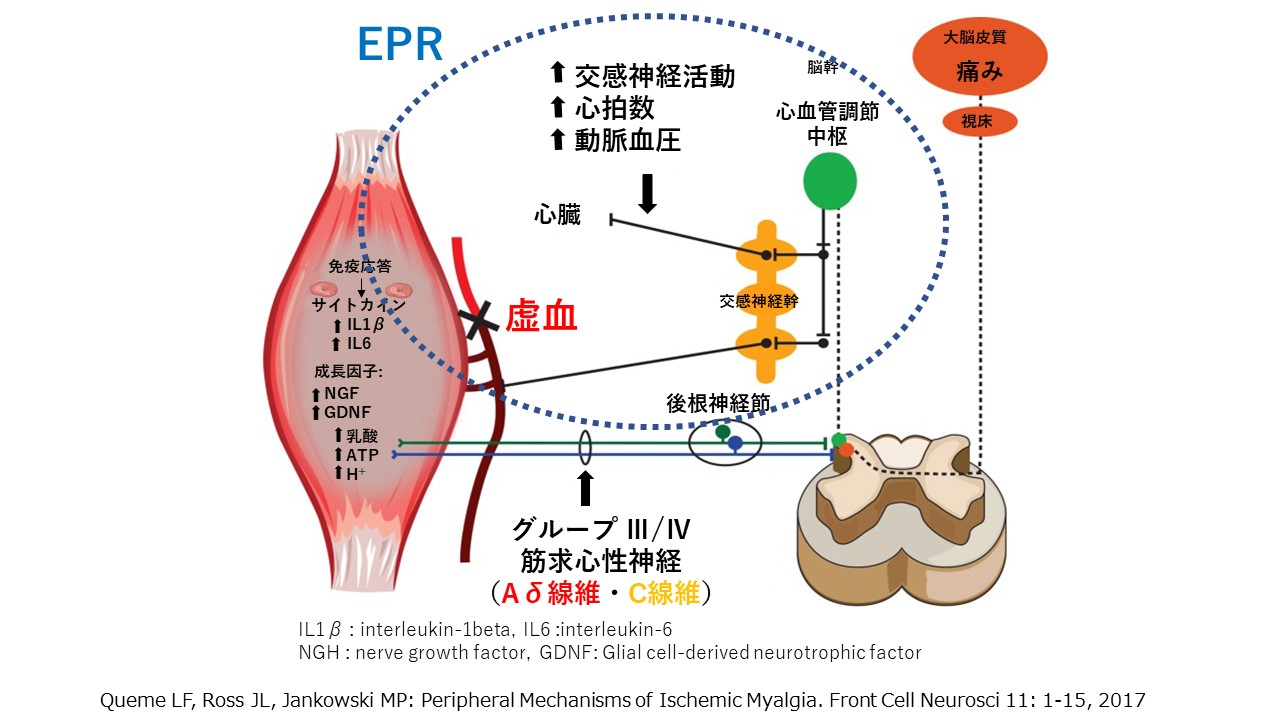
運動昇圧反射(exercise pressor reflex :EPR)
筋の虚血性損傷が起きると、Ⅲ群(Aδ線維)とⅣ群(C線維)の筋求心性神経からの情報は、脊髄を経て、
脳幹の心血管調節中枢の複数の核を活性化し、
脊髄の交感神経節前線維および交感神経幹を通り、心血管系の反応を調節します
つまり、筋に多くの血液を送るために、筋から発した情報が心血管調節中枢に直接働きかけるということです。
このことを運動昇圧反応(exercise pressor reflex :EPR)といいます。
しかし、虚血性筋痛(IM)においては、後根神経節(DRG)内の受容体が過剰発現(末梢?性感作)し、
このことによりEPRが誇張され(exaggerated EPRs)、交感神経が持続的に過緊張し、
同時に、痛みの中枢への伝達が強くなり、
虚血性損傷の臨床的に重要な合併症になる可能性があります。
Queme LF, Ross JL, Jankowski MP: Peripheral Mechanisms of Ischemic Myalgia. Front Cell Neurosci 11: 1-15, 2017
虚血性筋痛(IM)の後根神経節(DRG)における感作
虚血性損傷を来した筋ではNGF、グリア細胞株由来神経栄養因子(glial cell line-derived neurotrophic factor:GDNF)およびIL(interleukin)1βなどの炎症サイトカインなどが発生しⅢ・Ⅳ群線維(Aδ・C線維)の自由神経終末や後根神経節を刺激します。
そして虚血性損傷を来したそれらの神経の後根神経節では多様なチャネルや受容体が発現し痛みの末梢性感作(peripheral sensitization:以下PS)に関連します。

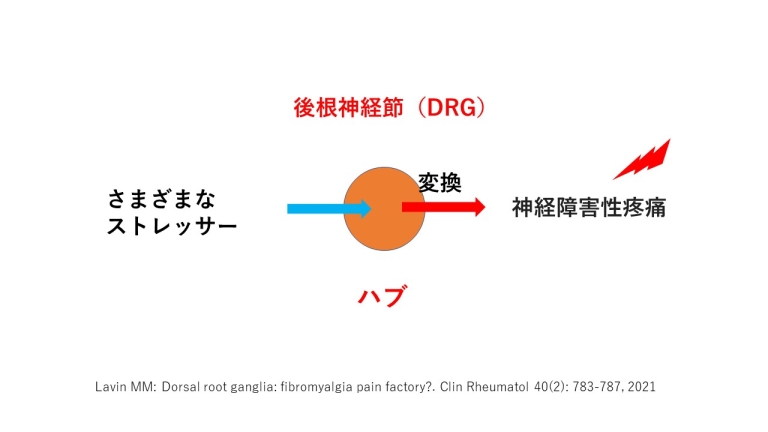
後根神経節(DRG)は線維筋痛症(FM)の痛みの工場?
Dorsal root ganglia : fibromyalgia pain factory?(後根神経節は線維筋痛症の痛みの工場?)と
いうタイトルの論文が報告されました。
Lavin MM: Dorsal root ganglia: fibromyalgia pain factory?. Clin Rheumatol 40(2): 783-787, 2021
後根神経節(DRG)は、さまざまな生体へのストレッサーを神経障害性の痛みに変えてしまう、まるでハブ(hub)のようです。
★ハブ(hub):中心、中核のことです。
私の、育った奄美大島や、大学時代と若い医師時代を過ごした沖縄にもハブがいましたが‥‥‥。
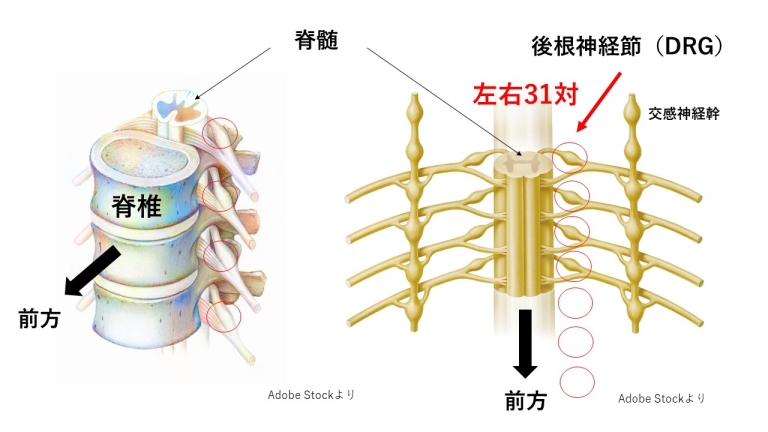
後根神経節(DRG)は、脊髄の近くに左右31対存在しています。

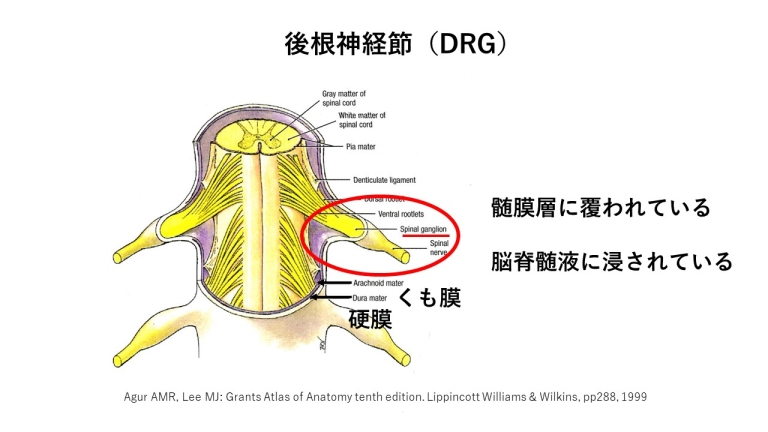
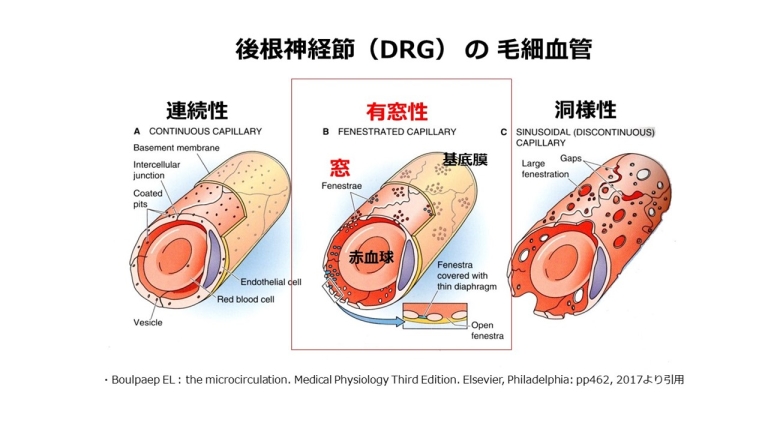
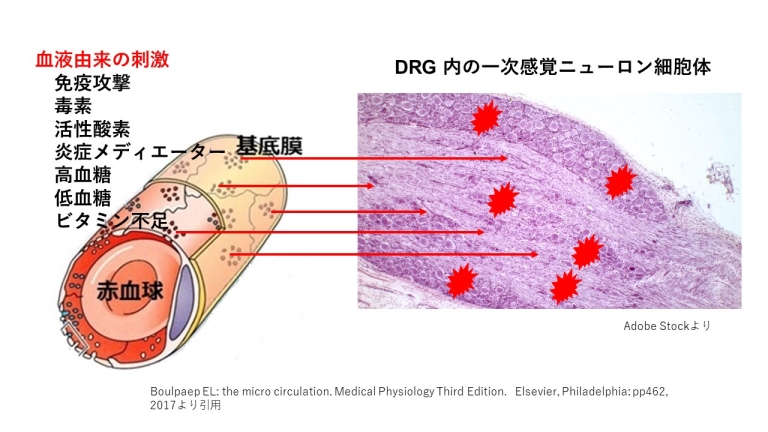
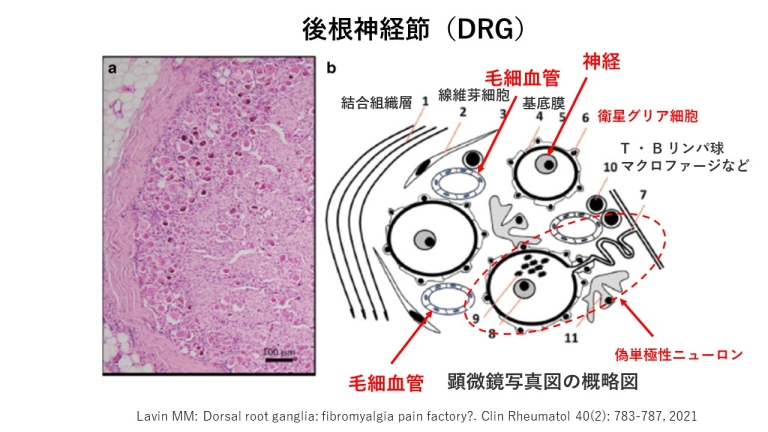
後根神経節(DRG)が障害を受ける原因を下に示します。
身体を守るために真っ先に反応する器官として発達したのだと考えます。
しかし、強い痛みはヒトを苦しめてしまいます。
そこまで痛みを感じるシステムを創らなくてもよかったのに、進化のミスマッチなのか?
後根神経節(DRG)のせっかくの情報を、まともに受け取ることのできない、未発達の脳のせいなのか?
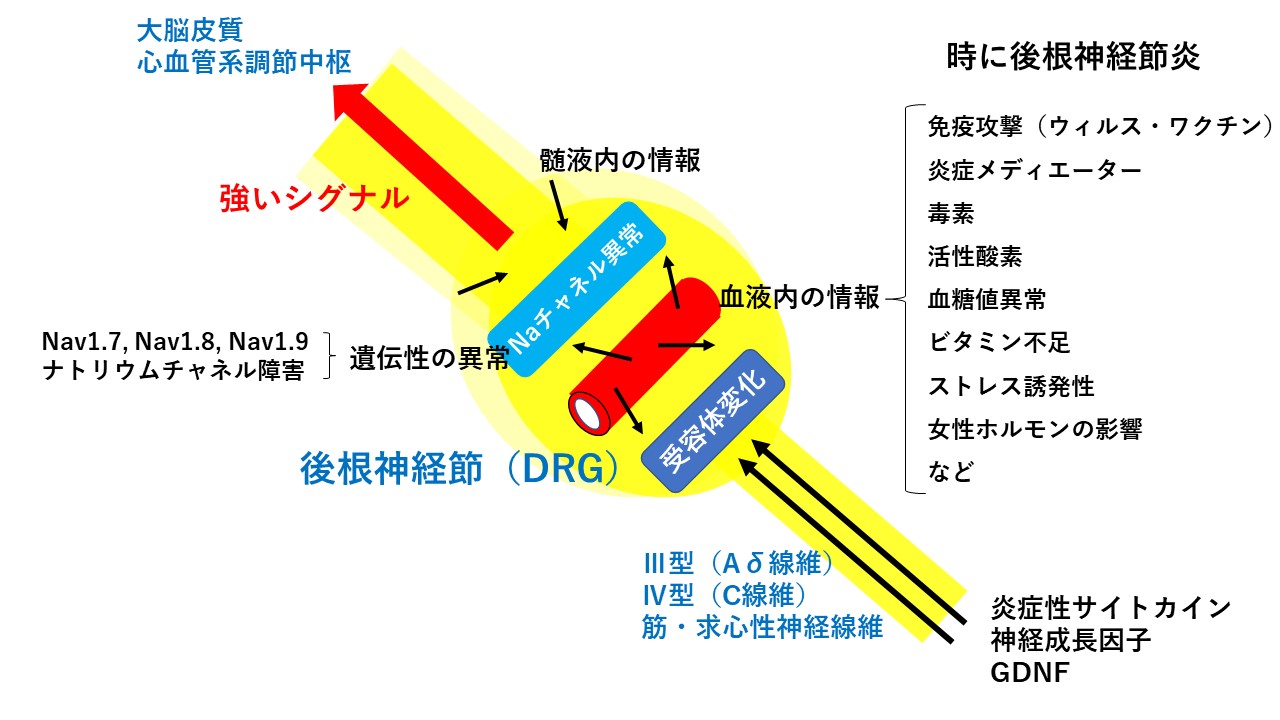
線維筋痛症(FM)における末梢病態としての虚血性筋痛(IM)
器質的原因のない線維筋痛症における、末梢病態としての虚血性筋痛(IM)は、特に、小心臓症など心血管系の先天的な脆弱性要因に、小径線維ニューロパチー(SFN)による神経障害性微小血管障害が、虚血・再灌流障害(IRI)を引き起こし、筋間質液成分が変化し、そのことにより筋(fascia)のⅢ型(Aδ線維)とⅣ型(C線維)の求心性感覚神経の興奮に至り、痛みとして大脳皮質に投影されます。時に、皮膚などに分布するAδ線維やC線維の後根神経節(DRG)が刺激され、全身のどこかに不規則なパッチ上の感覚障害が出現します。
小径線維ニューロパチー(SFN)による神経障害性微小血管障害と心血管系自律神経障害、および心筋代謝障害による心拍出量の低下は、起立不耐症、労作不耐症、脳の霧(brain fog)および多彩な身体症状を引き起こします。
また、損傷した筋組織内に成長因子や炎症サイトカインが放出されると、次第に、筋の求心性感覚神経であるⅢ型(Aδ線維)とⅣ型(C線維)の後根神経節(DRG)内の受容体の過剰発現(末梢性?感作)に至り、このことが誇張された運動昇圧反射(exaggerated EPRs)による持続的な交感神経の過緊張と増幅された痛みを引き起こし、さらに労作不耐症を悪化させます。
‥今のところ、このように考えています。

線維筋痛症(FM)の診断基準および臨床評価など
線維筋痛症(FM)の診断基準、分類基準、臨床評価は多数あり、どの基準が最も病態を反映し、臨床の現場で有用なのかは、現在も議論されています。
アメリカリウマチ学会(ACR)が公式に認めているものは、現在のところ、1990年分類基準および2010年診断基準です。
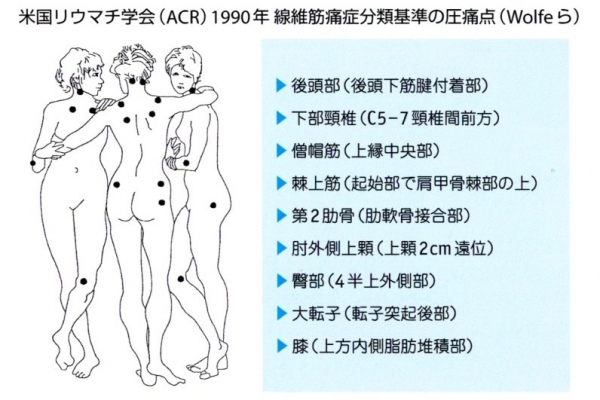
米国リウマチ学会(ACR)1990年 線維筋痛症分類基準の圧痛点(Wolfeら)
1,「広範囲の疼痛」の既往がある
定義
・疼痛は以下のすべてが存在するとき「広範囲の疼痛」とされる
・身体左側の疼痛、身体右側の疼痛、腰から上の疼痛、腰から下の疼痛さらに体幹中心部(頸椎、前胸部、胸椎、腰椎のいずれかの痛み)が存在する
2,手指による触診で18箇所の圧痛点部の11箇所に圧痛を認める
定義
・約4kgの強さの手指による触診で、下図に示した合計18箇所の圧痛点のうち11箇所以上に疼痛を訴える
判定
上記の2項目を認める場合に、線維筋痛症と診断(分類)される。
「広範囲の疼痛」は少なくとも3か月以上持続する必要がある
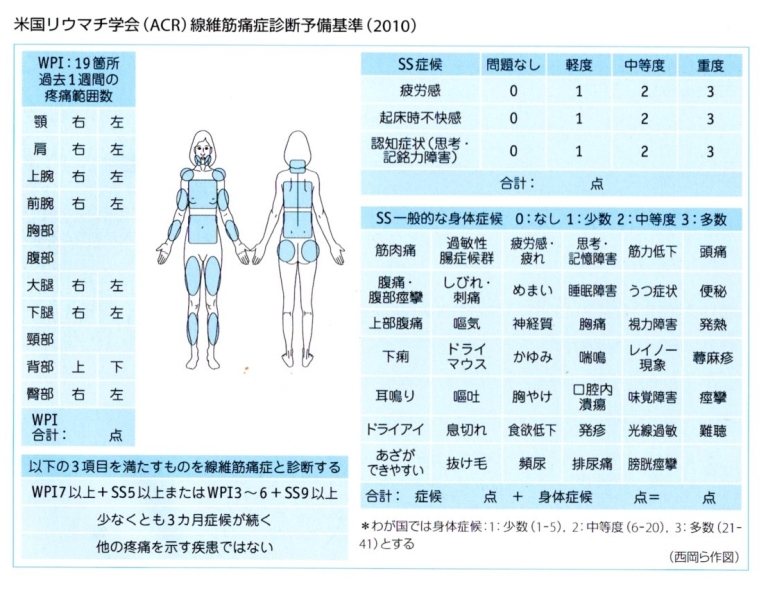
米国リウマチ学会(ACR)診断予備基準(2010)
2010年診断基準は以下の3項目からなります。
①定義化された慢性疼痛の広がり(疼痛拡大指数:widespread pain index: WPI)が一定以上あり、かつ臨床SSスコアが一定以上あること。
②臨床徴候が診断時と同じレベルで3か月間は持続すること。
③慢性疼痛を説明できる他の疾患がないこと。
この3項目を満たす場合に線維筋痛症(FM)と診断できる。
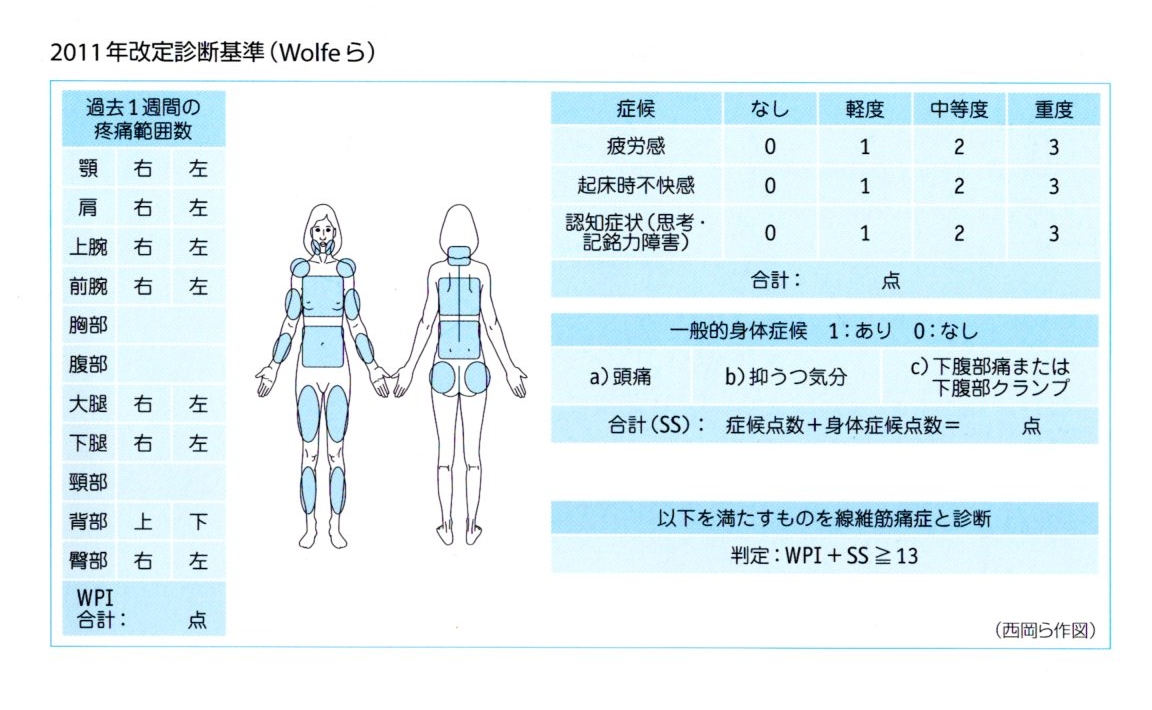
2011年改訂診断基準(Wolfeら)
2016年改訂診断基準(Wolfeら)
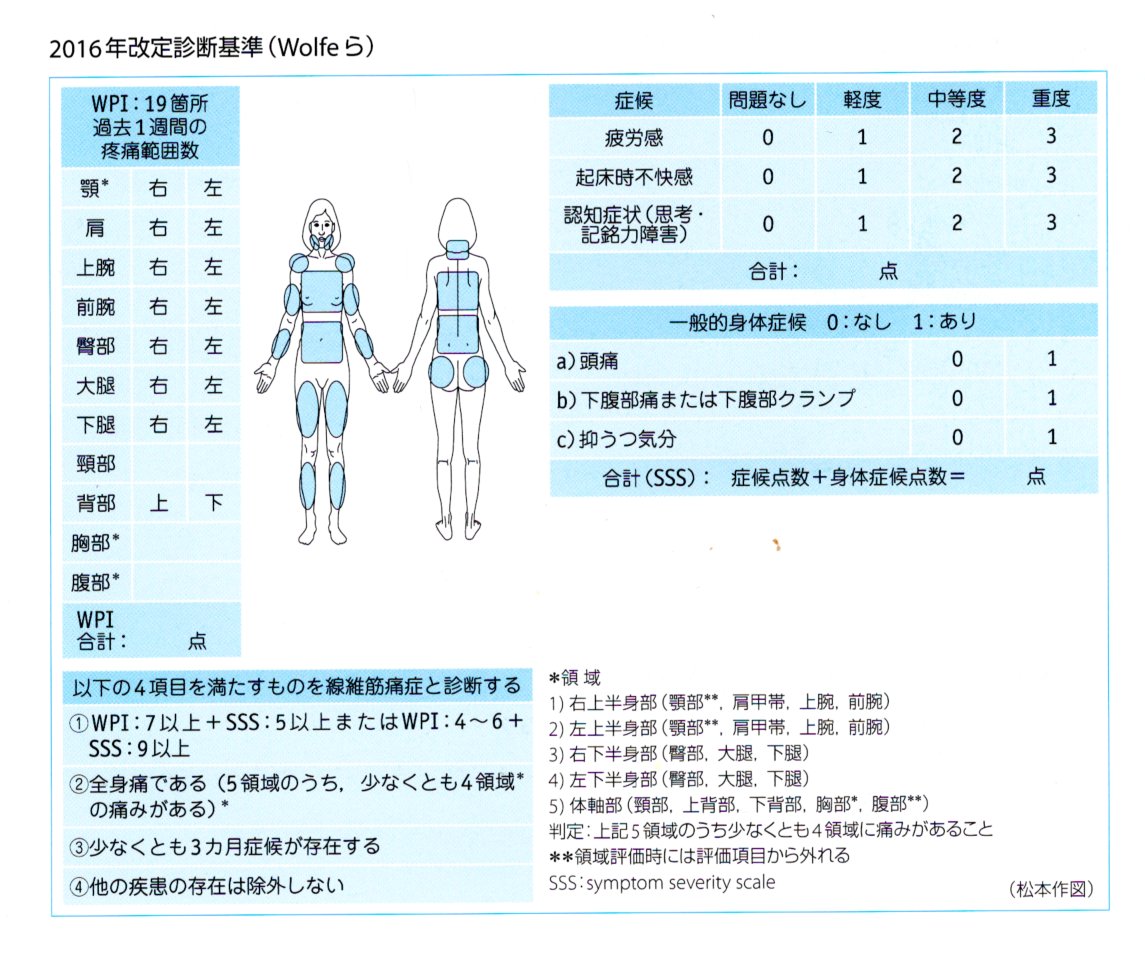
FAS31を用いた診断および疾患活動性の評価のための問診票
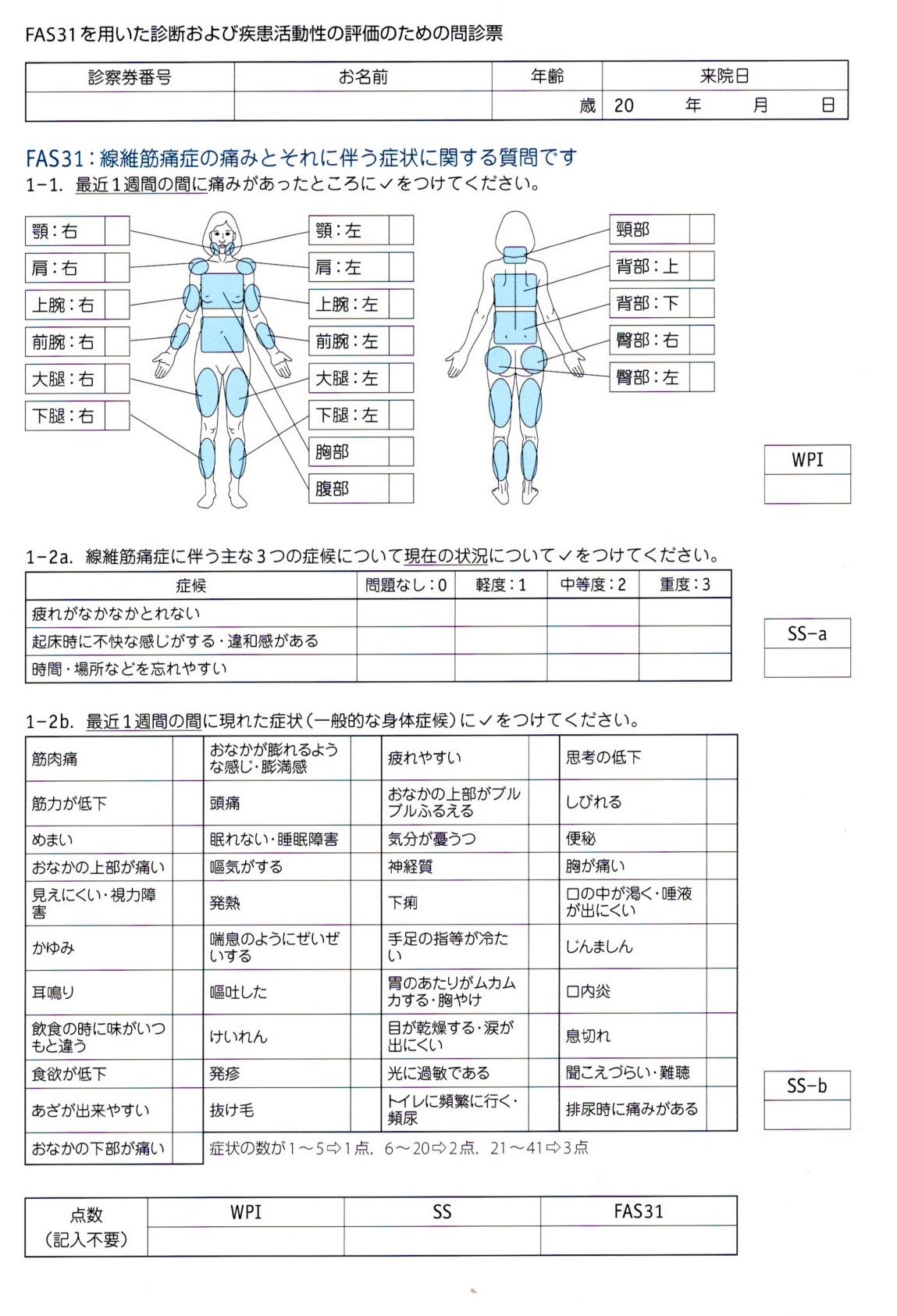
線維筋痛症質問表(JFIQ: The Japanese version of the FIBROMYALGIA IMPACT QUESTIONNAIRE)

線維筋痛症の AAPT(ACTTION-APS)診断基準
米国食品医薬品局(FDA)および米国疼痛学会(APS)とのACTTIONの官民パートナーシップ
ACTTION: The Analgestic, Anesthetic, and Addiction Clinical Trial Translation Innovations Opportunities and Networks
鎮痛薬・麻酔薬・依存症、臨床試験の翻訳、イノベーション、機会、ネットワーク
FDA:Food and Drug Administration(米国食品医薬品局)
APS:American Pain Society(米国疼痛学会)
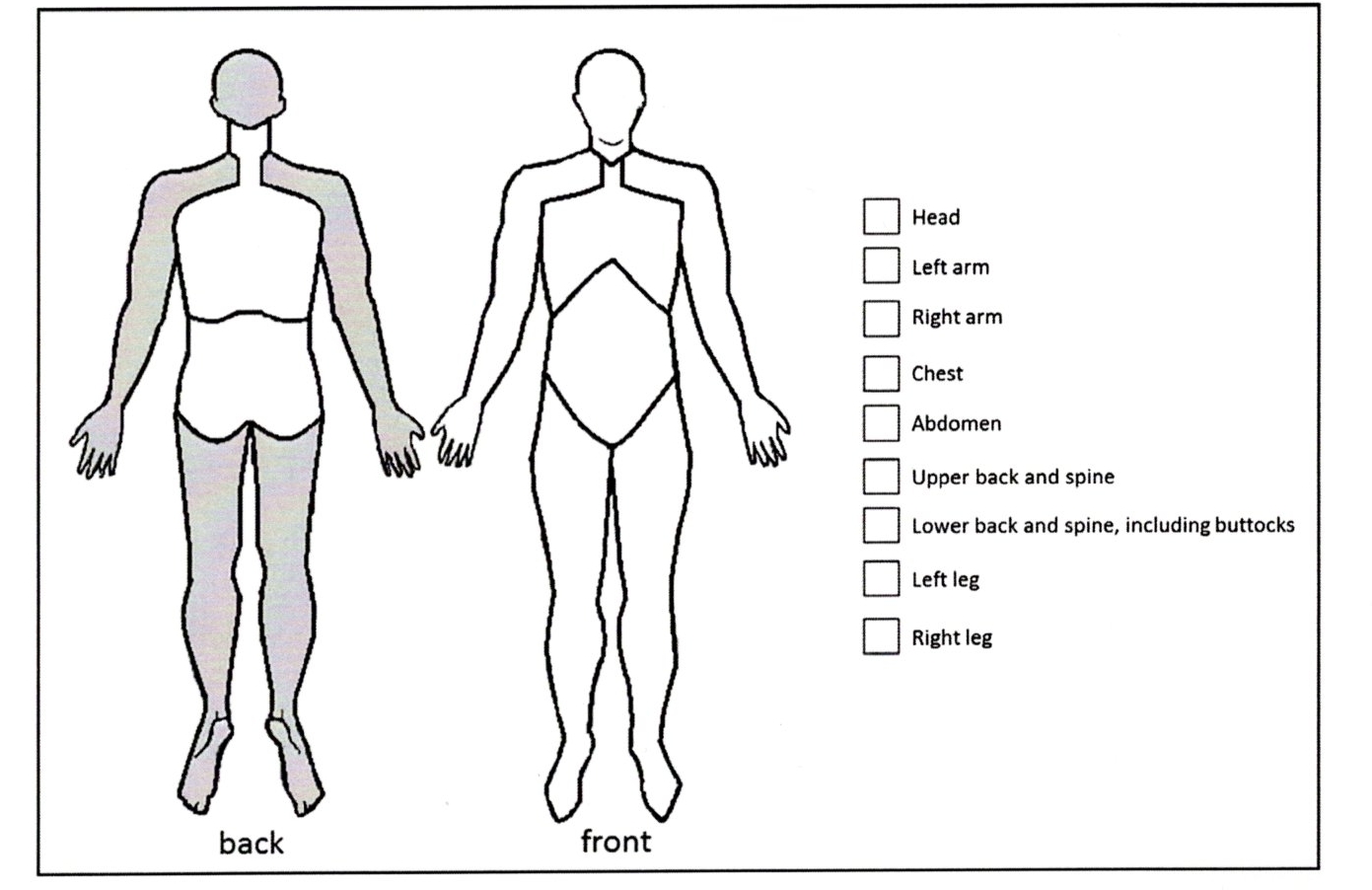
痛みを感じる体の部位の数患者には、2面体人型イラストの痛みを感じる部位にチェックを入れてもらう(あらかじめ網掛けしてある部位は無視する)。あるいは、患者は身体部位のチェックリストを使用してもよい。最大9つの身体部位から別々の部位の数を合計する。
次元1:コア診断基準
1. 9つの疼痛部位のうち、6つ以上の疼痛部位がMSP(multisite pain :複数部位の疼痛)と定義される
2. 中等度から重度の睡眠障害または疲労
3. MSPと疲労または睡眠障害が少なくとも3ヶ月以上続いていること
注 他の疼痛疾患や関連症状があっても、FM の診断が否定されることはない。
FM の診断を否定するものではない。しかし、患者の症状を十分に説明しうる、または重症化させる可能性のある疾患を評価するために、臨床評価を行うことが推奨される。
しかし、患者の症状を完全に説明できる、または症状の重篤度に寄与する可能性のある疾患を評価するために、臨床評価を行うことが推奨される。
Arnold L, Bennet R, Crofford L , et al : AAPT Diagnosis Criteria for Fibromyalgia. The Journal of Pain 20(6): 611-628, 2019
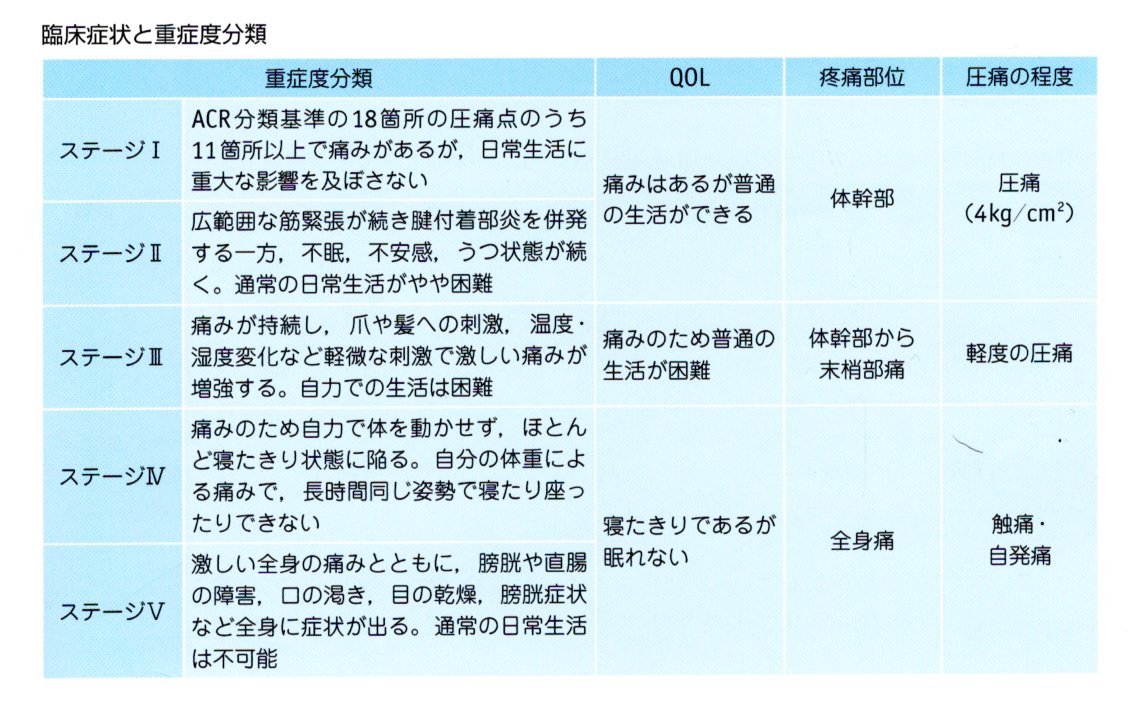
線維筋痛症(FM)の臨床症状と重症度分類
ステージⅠからステージⅤまでの段階は、
身体的苦悩(BD)から慢性機能障害性身体的苦痛(CDBD)へ至る段階と一致すると考えられます。
ステージⅠの段階、その前の段階で、
治療介入ができると回復可能性が高いと考えられます。
若年性線維筋痛症診断基準

線維筋痛症(FM)の治療
線維筋痛症(FM)の治療は、ガイドラインで示されています。調べるとすぐにいろいろな薬物治療が勧められています。
また、いろいろな代替医療が行われています。
多くは、痛覚変調性疼痛(nociplastic pain:NP)もしくは慢性機能障害性身体的苦悩(chronic disability bodily distress:CDBD)に至ったステージの治療と考えられます。
できるだけ早期に、身体的苦悩(bodily distress:BD)つまり、可逆性の初期・特発性・小径線維ニューロパチー(initially ideopathic SFN:iiSFN)および虚血性筋痛(IM)のステージの時期にホメオスタシスの歪みを改善する治療および身体症状から引き起こされる心理反応に対する適切なカウンセリングを行うことが大切であると考えます。








